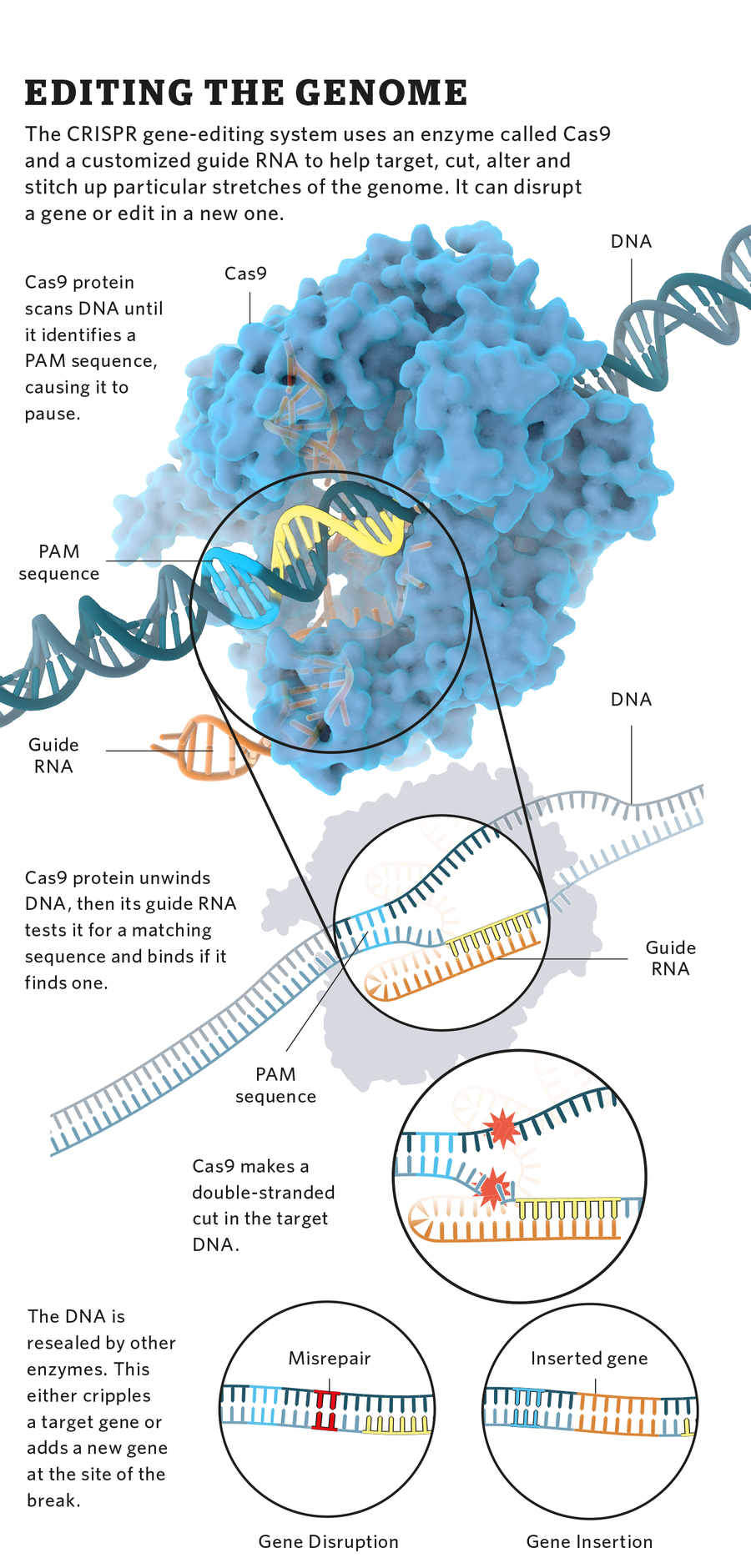
它最初是為了瞭解微生物如何抵抗病毒感染。在它們的染色體中,細菌儲存著從它們遇到的病毒中獲取的DNA片段。這些片段被一組稱為CRISPR(成簇的規律間隔的短迴文重複序列)的DNA片段標記,作為過去感染的記錄,並使細菌對未來的感染免疫。
對於詹妮弗·杜德納,一位HHMI研究員,加州大學伯克利分校的化學、生物化學和分子生物學教授,最大的問題是,這個系統是如何工作的?答案在於一種名為Cas9的酶。杜德納和她的團隊發現,當配備了病毒照片的RNA副本時,Cas9酶可以識別並停用攜帶匹配序列的病毒。
一旦她理解了這個系統,杜德納就開始利用它。透過向Cas9酶提供她選擇的引導RNA,杜德納發現她可以比現有方法更輕鬆、更準確地編輯目標DNA。Cas9引導的切口可以使目標基因失活。它還可以為新的DNA(例如目標基因的改變版本)提供插入位點。
對這種CRISPR-Cas9系統的描述(發表於2012年的《科學》雜誌)引發了生物學和生物技術領域的革命。在短短七年裡,CRISPR已成為重要的研究工具,並激發了許多新創企業的誕生。這項技術有潛力改變基礎科學、改良農作物和治癒遺傳疾病。與此同時,它也引發了關於如何處理一種具有改變人類進化能力的技術的倫理問題。
2018年,杜德納和她的兩位同事,馬克斯·普朗克感染生物學研究所的埃瑪紐埃爾·沙爾龐捷教授和維爾紐斯大學的維吉紐斯·西克西斯教授,因其在CRISPR-Cas9方面的工作而被授予科維理奈米科學獎。
現在,杜德納概述了在CRISPR充分發揮其潛力之前需要解決的下一個重大問題。
什麼是CRISPR 2.0,我們如何開發它?
CRISPR技術的一個大問題是如何確保基因組編輯的準確性和效率,這意味著引入DNA的確切改變。目前,科學家可以在基因組的特定位置觸發對DNA的定向改變,但我們更難確保引入的確切改變型別。目前正在進行的一些研究,不僅在我的實驗室裡,而且在整個領域中:一是開發所謂的CRISPR-Cas蛋白的鹼基編輯版本。這意味著開發使用這些可程式設計酶的方法,不是切割DNA,而是實際上觸發序列中特定DNA鹼基的化學變化。有了這些鹼基編輯分子,我們可以減少細胞產生不必要改變的機會。這是一種非常精細的DNA序列操作,原則上可以治癒細胞中導致疾病的突變。
Falconieri Visuals 插圖
我們能否利用CRISPR-Cas9對抗傳染病?
人們對這個問題很感興趣,至少在研究環境中是這樣。您能否利用CRISPR-Cas系統的適應性免疫功能來保護其他型別的細胞免受病毒侵害?我認為這不太可能,至少在其目前的形式下是這樣,因為病毒具有顯著的適應和進化能力,可以抵抗諸如CRISPR-Cas所使用的靶向機制。另一方面,我認為是否有方法可以靶向對人類有害的傳染性細菌?絕對有。該領域的前沿之一是探索如何使用CRISPR-Cas系統來靶向一些對人類有害的細菌。
我們能否轉向微生物來尋找替代的基因編輯工具?
生物學中一個令人驚歎的問題是,我們星球上存在哪些微生物?許多科學家,包括我在加州大學伯克利分校的同事吉利安·班菲爾德,正在透過對其DNA進行測序,並整合有關其生活方式、社群夥伴和環境生態位的資訊來研究環境中的微生物。我認為像我這樣的生物化學家和結構生物學家可以與DNA宏基因組學專家合作,嘗試瞭解這些生物體中的分子途徑。其中一些途徑提供了針對病毒的防禦,就像CRISPR系統一樣。CasX是CRISPR-Cas的新迭代版本,可以像Cas9一樣被程式設計來尋找和切割DNA。但它體積小得多,並且具有完全不同的分子形狀,因此可能更容易將其輸送到細胞中,並確保其進行臨床使用所需的準確編輯。
我們如何確保基因編輯惠及所有人?
很快,我們將面臨許多操縱DNA的機會——不僅在個體中,而且在可以將改變傳遞給後代的細胞中。鑑於此,我希望看到更多公眾與科學家互動的機會,以及更多探索基因編輯更廣泛影響的機會。它如何影響我們在社會上看到的不平等?它如何影響人們關於生殖和遺傳疾病的決定?我們如何定義遺傳疾病?我們認為什麼是健康,什麼是疾病?這些問題需要公開辯論。
要收聽與詹妮弗·杜德納的完整播客,請觀看下面的影片。


