我們對大腦如何利用耳朵之間兩磅半的鬆弛肉來完成學習的概念,可以追溯到伊萬·巴甫洛夫的經典實驗,他在實驗中發現狗可以學會聽到鈴聲就流口水。1949年,心理學家唐納德·赫布改編了巴甫洛夫的“聯想學習規則”,以解釋腦細胞如何獲取知識。赫布提出,當兩個神經元同時放電,同時發出脈衝時,它們之間的連線——突觸——就會變得更強。當這種情況發生時,就發生了學習。在狗的例子中,這意味著大腦現在知道鈴聲之後會立即出現食物。這個想法產生了一句經常被引用的格言:“一起放電的突觸連線在一起。”
該理論被證明是合理的,並且已經深入描述了學習過程中突觸如何變化的分子細節。但並非我們記住的所有事物都來自獎勵或懲罰,事實上,大多數經歷都會被遺忘。即使突觸確實一起放電,它們有時也不會連線在一起。我們保留什麼取決於我們對體驗的情感反應,它的新穎程度,事件發生的時間和地點,以及我們在事件期間的注意力和動機水平,我們會在睡眠時處理這些想法和感受。狹隘地關注突觸使我們對學習及其產生的記憶如何運作僅僅有了一個簡筆畫的概念。
事實證明,除了簡單迴路中最基本的反射之外,僅僅加強突觸本身並不能產生記憶。大腦範圍內的巨大變化對於創造連貫的記憶是必要的。無論您是在回憶昨晚與晚餐客人的談話,還是使用諸如騎腳踏車之類的習得技能,您大腦中許多不同區域的數百萬神經元的活動都必須聯絡起來,才能產生一個連貫的記憶,該記憶交織著情感、視覺、聲音、氣味、事件序列和其他儲存的體驗。由於學習涵蓋了我們經驗的許多要素,因此它必須包含突觸變化之外的不同細胞機制。這種認識導致人們開始尋找新的方法來理解資訊如何在人腦中傳輸、處理和儲存以實現學習。在過去的10年中,神經科學家已經意識到,構成大腦外表面的標誌性“灰質”——從教科書到兒童卡通等隨處可見的圖形插圖中都很熟悉——並非是器官中唯一參與永久記錄事實和事件以供日後回憶和重播的部分。事實證明,深埋在深深摺疊的灰色表面之下的區域也在學習中起著關鍵作用。就在過去幾年中,我和其他實驗室的一系列研究闡明瞭這些過程,這些過程可能為治療學習障礙引起的精神和發育障礙指明新的方向。
支援科學新聞
如果您喜歡這篇文章,請考慮支援我們屢獲殊榮的新聞報道,方式是 訂閱。透過購買訂閱,您正在幫助確保關於塑造我們今天世界的發現和想法的具有影響力的故事的未來。
如果僅憑突觸變化還不夠,那麼當您學習新事物時,您的大腦內部會發生什麼? 磁共振成像方法現在使研究人員能夠看穿人的頭骨並檢查大腦的結構。在仔細檢查 MRI 掃描時,研究人員開始注意到具有特定高度發達技能的個體的大腦結構差異。 例如,音樂家比非音樂傢俱有更厚的聽覺皮層區域。 起初,研究人員推測,這些細微的差異一定是使單簧管演奏家和鋼琴家有天賦擅長他們給定的技能。 但是隨後的研究發現,學習會改變大腦的結構。
導致腦組織改變的學習型別不僅限於重複的感覺運動技能,例如演奏樂器。神經科學家 Bogdan Draganski,目前在瑞士洛桑大學工作,他的同事們目睹了醫學生的灰質體積在他們為考試學習後增加。許多不同的細胞變化可能會擴大灰質體積,包括新神經元和稱為神經膠質的非神經元細胞的誕生。血管變化以及從神經元主體延伸出來的軸突和樹突的萌芽和修剪也可能做到這一點。值得注意的是,學習期間大腦的物理變化可能比預期的發生得更快。特拉維夫大學的 Yaniv Assaf 和他的同事表明,在一個計算機影片遊戲中,在賽道上跑 16 圈就足以引起新玩家海馬腦區的變化。這些遊戲玩家海馬體的結構改變是有道理的,因為這個大腦區域對於導航的空間學習至關重要。在其他研究中,Assaf 和牛津大學的 Heidi Johansen-Berg 分別驚訝地發現大腦中意想不到的部位發生了變化,包括沒有神經元或突觸的區域——稱為白質的區域。
深度學習
意識產生於大腦皮層,即人腦三毫米厚的表層,因此這個灰質層是大多數研究人員期望找到學習引起的修改的地方。但在表面層之下,數十億束緊密堆積的軸突(神經纖維),很像棒球皮革皮膚下的緊密纏繞的纖維,將灰質中的神經元連線成迴路。
這些纖維束是白色的,因為軸突塗有一層稱為髓磷脂的脂肪物質,髓磷脂充當電絕緣體,並將傳輸速度提高 50 到 100 倍。白質損傷和疾病是重要的研究領域,但直到最近,這些研究中很少有人關注髓磷脂在資訊處理和學習中可能起的作用。
在過去的 10 年左右的時間裡,研究已經開始發現在具有各種技能的專家的腦部掃描中,包括在閱讀和算術方面具有高超技能的人,白質存在差異。與新手相比,高爾夫球專家和訓練有素的雜耍演員也表現出白質的差異,並且白質體積甚至與智商有關。如果資訊處理和學習源於灰質中神經元之間突觸連線的加強,為什麼學習會影響大腦的皮下佈線?
一個可能的答案開始從我的實驗室進行的細胞研究中浮現出來,該研究調查了突觸——以及其他大腦區域——在學習過程中如何變化。 關注突觸之外的原因是,我們目前用於治療神經和心理疾病的大多數藥物都是透過改變突觸傳遞來發揮作用的,並且迫切需要更有效的藥物。 目前對突觸傳遞的關注可能會使我們失去獲得治療痴呆症、抑鬱症、精神分裂症或創傷後應激障礙 (PTSD) 的更好療法的機會。
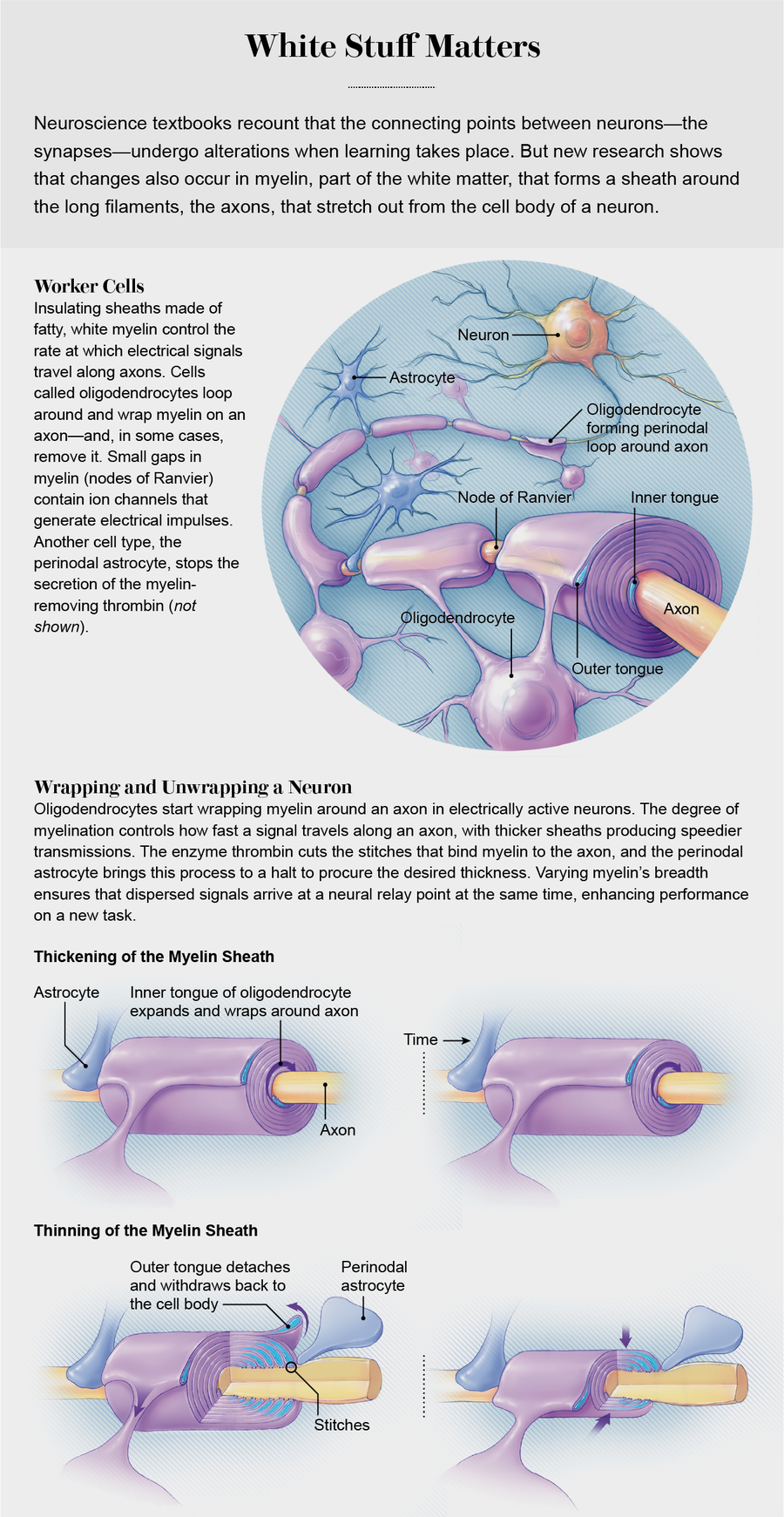
圖片來源:David Cheney;來源:“髓鞘可塑性的跑步機模型”,R. Douglas Fields 和 Dipankar J. Dutta 合著,發表於 Trends in Neurosciences,第 42 卷; 2019 年 7 月
在 1990 年代初期,我在美國國立衛生研究院的實驗室和其他實驗室開始探索神經膠質細胞可能能夠感知流經神經網路的資訊並改變它以提高效能的可能性。 自那時以來積累的實驗證據表明,所有型別的神經膠質細胞都對神經活動做出反應,並且可以改變大腦中的資訊傳遞。 這些新發現中最令人驚訝的之一涉及髓磷脂。
髓磷脂絕緣層是由包裹在軸突周圍的細胞膜層(如電工膠帶)形成的。 在大腦和脊髓中,章魚狀的神經膠質細胞(少突膠質細胞)進行包裹。 在四肢和軀幹中,香腸狀的神經膠質細胞(雪旺細胞)執行相同的任務。 許多少突膠質細胞抓住軸突並在其周圍包裹髓磷脂層,就像棒球運動員疊放雙手抓住球棒以確定哪支球隊先擊球一樣。 兩個髓磷脂節段之間微小的間隙暴露了一個一微米長的裸軸突部分,在該部分中,產生電脈衝的離子通道變得集中。 這些空間稱為郎飛結,就像生物電中繼器一樣,將電脈衝從一個結中繼到另一個結,沿著軸突向下傳遞。 隨著更多層髓磷脂包裹在軸突周圍,脈衝傳輸速度會提高,從而更好地防止電壓損失。 此外,隨著郎飛結被相鄰的髓磷脂節段更緊密地擠壓,電脈衝的啟動速度更快,因為將較小量的結膜充電到觸發離子通道開啟併產生脈衝的電壓所需的時間更少。
破壞髓磷脂的疾病,如多發性硬化症和格林-巴利綜合徵,可能會導致嚴重的殘疾,因為當絕緣層受損時,神經脈衝傳遞會失敗。 但直到最近,髓磷脂可能會被神經脈衝常規修飾的想法還沒有被廣泛接受。 即使髓磷脂結構發生變化,這將如何以及為何提高效能和學習能力?
解釋就隱藏在眼前。 它回到了關於神經元放電和連線在一起的舊格言。 在任何複雜的資訊或傳輸網路中,到達網路中繼點的時間至關重要——想想因為您的航班到達太晚而錯過轉機。
那麼,人腦中每個鏈路的傳輸速度如何適當地定時,以便脈衝在需要時及時到達? 我們知道,在某些軸突中,電訊號以緩慢的步行速度緩慢移動,而在另一些軸突中,電訊號則以賽車的速度快速移動。 除非最佳化來自兩個軸突的輸入源的行程時間以補償兩個軸突長度的差異以及脈衝沿著每個鏈路傳播的速度,否則匯聚在充當中繼點的神經元上的訊號不會同時到達。
由於髓磷脂是提高脈衝傳輸速度的最有效手段,因此軸突髓鞘形成促進了透過網路的最佳資訊傳輸。 如果少突膠質細胞感知並響應流經神經迴路的資訊流量,那麼髓磷脂的形成及其調整脈衝傳輸速度的方式可以受到來自軸突的反饋控制。 但是髓鞘化神經膠質細胞如何檢測流經軸突的神經脈衝?
訊號傳輸
在過去的二十年中,我們實驗室和其他實驗室的研究成功地鑑定了許多神經遞質和其他訊號分子,這些分子將軸突中存在電活動的資訊傳遞給神經膠質細胞,以刺激髓鞘形成。 我們的實驗表明,當神經元放電時,神經遞質不僅在突觸處釋放,而且沿著軸突也釋放。 我們發現,章魚狀少突膠質細胞的“觸手”探測軸突的裸露部分,以尋找從放電軸突釋放的神經遞質。 當單個觸手接觸正在放電的軸突時,它會形成“點焊”接觸,從而實現軸突和少突膠質細胞之間的通訊。 少突膠質細胞開始在該點合成髓磷脂並將其包裹在軸突周圍。
當我們在細胞培養物中給少突膠質細胞選擇髓鞘化電活動軸突或用肉毒桿菌毒素處理以阻止神經遞質釋放的軸突時,少突膠質細胞以八比一的比例選擇了電活動軸突而不是沉默軸突。 因此,當一個人學習在鋼琴上演奏《致愛麗絲》時,在練習期間重複啟用的迴路中,裸軸突可能會被髓磷脂包裹,或者現有髓鞘的體積會增加,從而加快資訊流過大腦網路的速度。 然後,新的髓磷脂會在 MRI 上顯示為大腦中音樂表演必要部分的白質束的變化。
幾個實驗室已經證實,動作電位,即沿著軸突長度傳遞的訊號,會刺激這些神經佈線暴露區域的髓鞘形成。 2014 年,Michelle Monje 在斯坦福大學的實驗室表明,光遺傳學刺激(使用雷射使神經元放電)增加了小鼠大腦中的髓鞘形成。 同年,William Richardson 在倫敦大學學院的實驗室證明,當阻止新的髓磷脂形成時,小鼠學習如何在輪子上跑步(輪子上移除了一些橫檔)的速度會變慢。 在他們使用共聚焦顯微鏡觀察活斑馬魚中髓磷脂形成的研究中,愛丁堡大學 David Lyons 實驗室和科羅拉多大學丹佛分校 Bruce Appel 實驗室的研究人員觀察到,當抑制軸突釋放包含神經遞質的小囊泡時,通常最初的幾層髓磷脂會滑落,少突膠質細胞會中止整個過程。
2018 年,我們與包括來自日本各機構的 Daisuke Kato 等同事合作,展示了髓磷脂如何透過確保沿著軸突傳播的各種尖峰電訊號同時到達控制運動的大腦區域運動皮層來促進學習。 透過使用轉基因髓鞘形成受損的小鼠(這些小鼠經過訓練以拉動槓桿以獲得獎勵),我們發現學習這項任務增加了運動皮層中的髓鞘形成。
透過使用電極記錄神經脈衝,我們發現髓鞘形成缺陷小鼠的運動皮層中的動作電位同步性較差。 然後,我們透過使用光遺傳學在適當的時間使神經元放電來提高運動皮層中尖峰到達的同步性。 髓鞘形成受損的小鼠隨後熟練地完成了學習的任務。 最終,侵入性較小的腦刺激形式可能成為治療由髓鞘形成中斷引起的神經和心理疾病的有效療法。
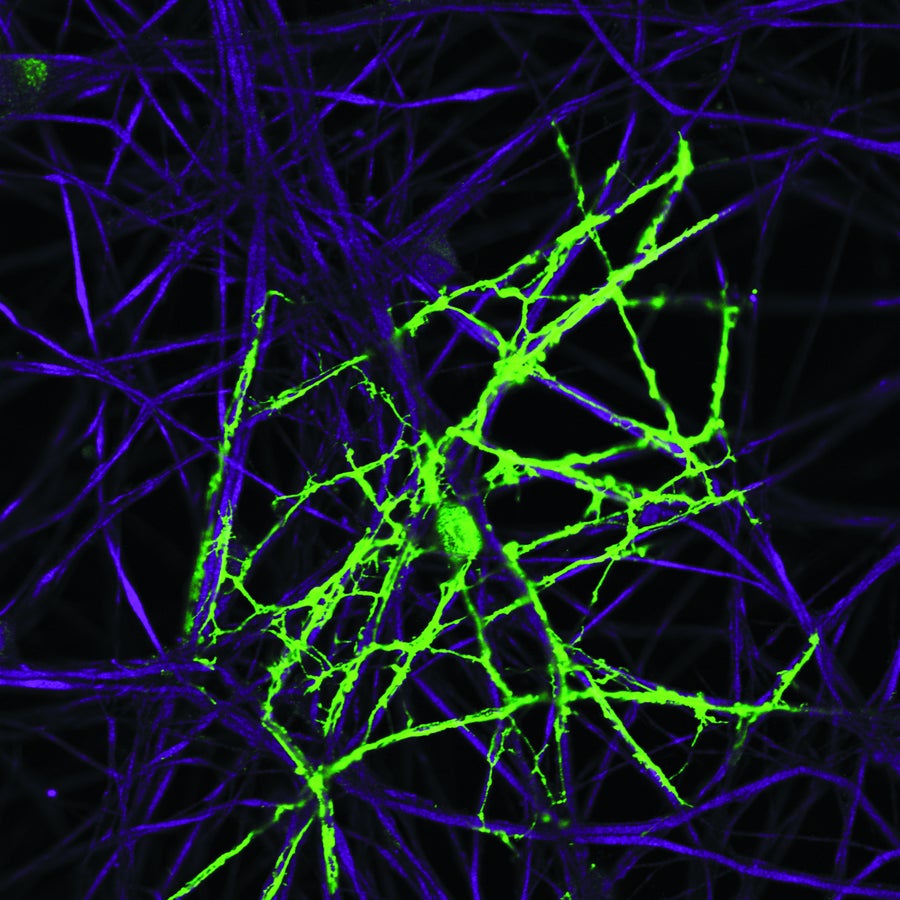
少突膠質細胞(綠色)準備用髓磷脂包裹軸突(紫色)。 圖片來源:R. Douglas Fields 美國國立衛生研究院和 NICHD
儘管最近取得了這些進展,但刺激以增加軸突髓鞘形成並不總是足以實現新的學習,因為我們無法透過簡單地使脈衝儘可能快速地傳播來同步神經網路中關鍵中繼點的尖峰到達時間。 還必須有一種方法來減慢那些過早到達這些點的輸入的脈衝速度。
必須以受控方式加厚或變薄已在軸突上形成的髓磷脂,以加快或減慢訊號傳輸速度。 在我們的發現之前,除了疾病損害之外,還沒有已知的解釋說明如何變薄髓鞘以減慢訊號速度。 我們的研究揭示了另一種參與這些“可塑性”神經系統變化的神經膠質細胞。
郎飛結周圍是一種稱為星形膠質細胞的神經膠質細胞。 星形膠質細胞具有許多功能,但大多數神經科學家在很大程度上忽略了它們,因為它們不透過電脈衝與其他細胞通訊。 令人驚訝的是,過去十年的研究表明,位於兩個神經元之間突觸附近的星形膠質細胞可以透過釋放或攝取神經遞質來調節學習期間的突觸傳遞。 但直到最近,髓磷脂生物學家才傾向於忽略在郎飛結處接觸軸突的獨特型別的星形膠質細胞。
這些所謂的結周星形膠質細胞到底做什麼來變薄髓鞘? 正如人們在改造服裝時開始做的那樣,這些細胞幫助切割“接縫”。 髓鞘透過位於郎飛結側面的螺旋連線附著在軸突上。 在電子顯微鏡下,這些連線看起來像是軸突和髓磷脂之間的螺旋縫線,形成每個縫線的線由三個細胞粘附分子複合物組成。 我們對這些縫合點的分子組成的分析表明,這些分子之一神經纖絲蛋白 155 具有一個可以被特定酶凝血酶切割以變薄髓磷脂的位點。
凝血酶由神經元產生,但也可以從血管系統進入大腦。 隨著髓磷脂從軸突上脫落,郎飛結處的裸軸突量增加。 髓磷脂的外層附著在與結周星形膠質細胞相鄰的軸突上。 當髓磷脂從軸突上脫離時,外層縮回到少突膠質細胞中,從而使髓鞘變薄。 結間隙的擴大和髓鞘的變薄都會減慢脈衝傳輸速度。
我們發現,酶對將髓磷脂縫合到軸突的這些線的剪下可以受到結周星形膠質細胞釋放的凝血酶抑制劑的控制。 我們對轉基因小鼠進行了實驗,在這些小鼠中,星形膠質細胞釋放的這種凝血酶抑制劑較少。 當我們用電子顯微鏡觀察它們的神經元時,我們可以看到髓磷脂變薄,並且結間隙增大。 透過使用電子放大器檢測神經脈衝並測量其傳輸速度,我們發現,在這種方式髓磷脂厚度降低後,視神經中的脈衝傳輸速度減慢了約 20%,並且動物的視力下降。 我們能夠透過注射凝血酶抑制劑來逆轉所有這些變化,這些抑制劑被批准用於治療血管疾病。
我們的實驗支援了一個新的假設:髓鞘厚度的變化代表了一種新的神經系統可塑性形式,這種可塑性受髓磷脂的新增和減去控制。 髓磷脂的附加層不會像人們將膠帶纏繞在電線上那樣新增到軸突上,因為這會將少突膠質細胞的腿打結。 相反,新的絕緣層是透過構建新的內層來固定的,該內層像蛇一樣在下面的髓磷脂下方螺旋纏繞在軸突周圍。 同時,髓磷脂的外層可以被結周星形膠質細胞分離以變薄髓鞘。 髓鞘的厚度不是固定的; 相反,它反映了軸突旁邊新增層和星形膠質細胞控制下外層去除之間的動態平衡。
大腦的波浪
中繼點處動作電位的最佳時間對於透過調整其時間以使其共同放電來加強突觸至關重要。 但髓磷脂可塑性可以透過另一種方式促進神經迴路功能和學習——透過調整腦波振盪的頻率。 大腦中的並非所有神經活動都來自感覺輸入。 其中大部分是由於大腦自身在有意識和無意識層面發生的事情而發生的。 這種自我產生的活動由不同頻率的振盪波組成,這些振盪波掃過大腦,就像汽車發動機在一定速度下的振動會使汽車的不同部件以共振頻率一起嘎嘎作響一樣。
這些腦波或振盪被認為是連線大腦遙遠區域神經元的關鍵機制,這對於分類和傳輸神經資訊可能很重要。 例如,振盪將前額葉皮層(提供上下文含義)和海馬體(負責編碼空間資訊)中的神經活動聯絡在一起。 這種振盪耦合使人能夠快速識別工作中熟悉的臉孔,但同時也使在不熟悉的地方識別同一位同事變得更加困難。
更重要的是,睡眠的各個階段(對於儲存長期記憶至關重要)可以透過以不同頻率振盪的腦波來識別。 我們白天積累的經驗在睡眠期間被重播,並根據它們與其他記憶和情感的關係進行分類以進行儲存或刪除,這些關係可以將它們標記為未來可能有用(或無用)。 適當的腦波振盪被認為是記憶鞏固過程中的關鍵。 但脈衝傳輸速度對於同步腦波至關重要。
正如兩個蹣跚學步的孩子必須精確地定時他們的腿部運動才能驅動蹺蹺板的上下運動一樣,兩組振盪神經元之間的傳輸延遲必須定時,以便耦合神經元在大腦中的長距離範圍內同步振盪。 髓磷脂可塑性對於腦波很重要,因為適當的傳導速度對於維持以相同頻率耦合大腦兩個區域的振盪是必要的。
這個結論是基於我和我的 NIH 同事 Sinisa Pajevic 和 Peter Basser 對波傳播基本物理學進行的數學建模得出的。 2020 年,多倫多大學 Paul Frankland 實驗室的 Patrick Steadman 和他的同事進行的一項研究為這個想法提供了令人信服的實驗支援。 研究人員使用了轉基因小鼠,在這些小鼠中,髓鞘形成可以暫時停止,他們發現學習恐懼不安全環境和記住安全位置的能力取決於新髓磷脂的形成。 此外,他們發現在這種型別的學習中,睡眠期間的腦波活動在海馬體和前額葉皮層之間變得耦合。 阻止新髓磷脂的形成還會削弱連線,並導致一種在創傷事件後難以將恐懼與適當背景聯絡起來的人身上經常發現的記憶障礙。
學習和執行任何複雜的任務都涉及不同大腦區域中許多不同神經元的協調運作,並且需要訊號以最佳速度透過大型神經網路。 髓鞘對於最佳傳輸至關重要,但人們在老年時開始失去大腦皮層中的髓磷脂。 這種逐漸退化是我們認知速度減慢以及隨著年齡增長學習新事物越來越困難的原因之一。
考慮一下傳輸延遲如何中斷電話的遠端通訊。 同樣,大腦中的延遲會導致精神分裂症等心理障礙患者出現認知困難和思維混亂。 事實上,在許多神經和精神疾病中都可以看到腦波振盪的差異。 例如,阿爾茨海默病與白質的變化有關。
控制髓磷脂產生的藥物可以為治療這些問題提供新的方法。 事實上,中國第三軍醫大學的王飛和他的同事與加州大學舊金山分校的 Jonah Chan 合作,在 2020 年報告稱,給予基因缺失小鼠(這種基因缺失會損害少突膠質細胞的發育)促進髓鞘形成的藥物克萊瑪汀改善了在水迷宮中測試的學習能力。 由於髓鞘形成受到多種形式的神經活動的影響,因此許多技術(例如,認知訓練、神經反饋和物理治療)可能有助於治療與年齡相關的認知能力下降和其他疾病。 韓國 Jung-Hae Youn 和他的同事在 2018 年對老年人進行的一項研究表明,為期 10 周的記憶訓練練習提高了回憶能力。 訓練前後的腦部成像顯示,接受記憶訓練課程的老年人群體中,連線到額葉的白質束的完整性有所提高。
這些新穎的概念已經開始改變我們思考大腦作為一個系統如何運作的方式。 髓磷脂長期以來被認為是軸突上惰性的絕緣層,現在被視為透過控制訊號沿神經佈線傳播的速度來為學習做出貢獻。 透過冒險超越突觸,我們開始填充突觸可塑性的簡筆畫骨架,以建立更全面地瞭解當我們學習時大腦中發生的事情的圖景。
