今年年初,當 COVID-19 疫情爆發時,費城郊外的一家小型製藥公司正在努力推銷一種可以幫助與死神搏鬥的患者的化合物。
Paratek Pharmaceuticals 公司花費了 20 多年時間開發和測試一種名為奧馬環素 (Nuzyra) 的抗生素,該抗生素於 2019 年在美國上市,用於治療細菌感染。儘管抗生素不能對抗引起 COVID-19 的病毒,但近 15% 的 COVID-19 住院患者會發展為細菌性肺炎,其中一些肺炎對現有抗生素具有耐藥性。
在 COVID-19 之前,據估計全球每年至少有 70 萬人死於抗生素耐藥性。隨著越來越多的病毒性疾病患者接受抗生素治療繼發感染,或預防因使用呼吸機而引起的感染,這個數字現在可能會攀升。這正是奧馬環素等藥物可能發揮作用的地方——如果它能及時送到人們手中以挽救生命的話。
支援科學新聞報道
如果您喜歡這篇文章,請考慮透過以下方式支援我們屢獲殊榮的新聞報道 訂閱。透過購買訂閱,您將幫助確保未來能夠繼續報道關於塑造我們當今世界的發現和想法的具有影響力的故事。
“COVID 是一次警鐘,”Paratek 執行長 Evan Loh 說,該公司在賓夕法尼亞州和馬薩諸塞州波士頓設有辦事處。他說,診斷、抗體和疫苗都是為應對疫情做準備的關鍵,“我們需要抗生素,讓人們有最好的機會從這種特殊感染中倖存下來。” 但生產抗生素的製藥商面臨著獨特的挑戰。
一個痛苦的悖論是,抗生素推動了 20 世紀利潤最高的製藥公司的發展,並且是社會最迫切需要的藥物類別之一。然而,抗生素市場卻已崩潰。近二十年來,曾經主導抗生素髮現的大型企業一直在逃離該業務,稱他們可以為這些救命藥物收取的價格太低,無法支援開發成本。現在從事抗生素研究的大多數公司都是小型生物技術公司,其中許多公司靠信貸運營,而且許多公司正在倒閉。
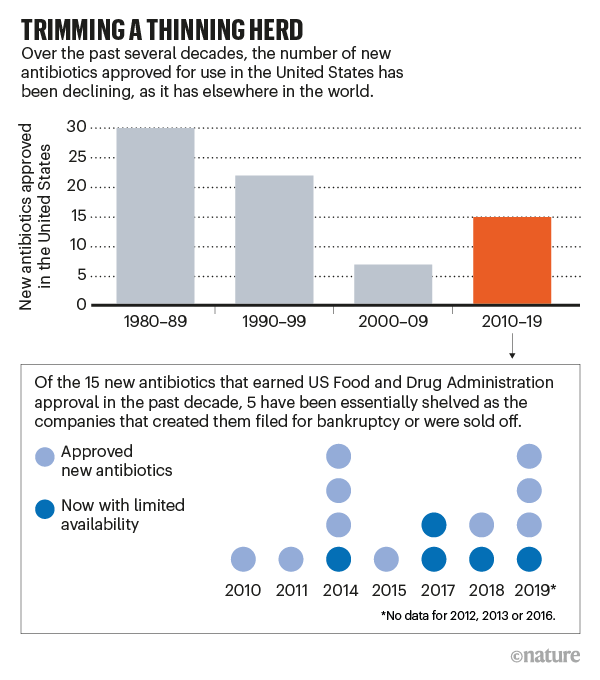
就在過去的兩年裡,四家這樣的公司宣佈破產或掛牌出售,儘管它們經歷了長達十年的危險的開發和測試過程,才獲得新藥批准。當 Achaogen、Aradigm、Melinta Therapeutics 和 Tetraphase Pharmaceuticals 倒閉時,它們從市場上撤下了——或大幅減少了——自 2010 年以來美國食品和藥物管理局 (FDA) 批准的 15 種抗生素中的 5 種(見“修剪日益稀少的畜群”)。
透過保守的支出、經驗和好運(包括去年年底獲得的一份利潤豐厚的政府合同),Paratek 迄今為止避免了將許多其他公司拉下水的退潮。但奧馬環素的收益雖然穩定,但尚未確保 Paratek 的長期生存。
“歸根結底,Paratek 仍然需要銷售一種藥物,”前製藥公司高管、現任抗生素開發顧問和作家 David Shlaes 說。“而且完全不清楚它是否能夠銷售足夠多的藥物來盈利。”

美國 Paratek Pharmaceuticals 公司執行長 Evan Loh 領導著一個團隊,該團隊正在努力確保一種新型抗生素的未來。圖片來源:Hannah Yoon,為《自然》雜誌拍攝
成本高昂的業務
將一種新型抗生素推向市場是一項艱鉅的任務。據世界衛生組織稱,只有約 14% 的處於 I 期臨床試驗階段的抗生素和生物製劑有可能獲得批准。一組經濟學家在 2016 年估計,從首次識別活性藥物分子到獲得美國 FDA 批准的成本為 14 億美元,批准後還需要數百萬美元用於營銷和監測。當禮來公司或默克公司在 20 世紀中葉生產抗生素時,這些成本可以在其多個部門分攤。而且,當大型公司像過去那樣收購新藥顯示出臨床前前景的小公司時,收購價格涵蓋了小公司產生的所有債務。
這些商業模式已不復存在。Paratek 的三人管理團隊深知這一點,因為他們都是大型公司的資深人士。Loh 曾在費城的惠氏製藥公司與 Paratek 總裁兼首席商務官 Adam Woodrow 以及首席開發和監管官 Randy Brenner 合作開發了成功的抗生素替加環素 (Tygacil),該抗生素於 2005 年獲得批准。(惠氏公司於 2009 年將其抗生素業務組合出售給了輝瑞公司。)
“當您從一家大公司來到一家小公司時,您的重點就變成了:‘我如何確保這家公司生存下去?’”Brenner 說,他之前也曾在紐約市的輝瑞公司和馬薩諸塞州列剋星敦的 Shire 公司(現為東京武田製藥公司的子公司)工作過。“大公司不需要這樣考慮。無論產品發生什麼,公司都會生存下去。”
替加環素基於四環素,這是最早的抗生素類別之一;它們於 1948 年首次使用,僅比青黴素問世晚六年。多年來,一代又一代的四環素上市,但都被耐藥性削弱了作用。替加環素的結構融入了一些調整,使其能夠避開這些耐藥機制,但這是有代價的:該藥物只能靜脈注射給藥。
這是一個侷限性。靜脈注射藥物通常會在醫院和醫療中心給藥,這使得藥物既更昂貴,又更不易為患者所用。因此,當替加環素正在開發時,醫生兼研究員 Stuart Levy——美國抗生素耐藥性研究的巨頭之一,在波士頓塔夫茨大學工作——提出配製另一種四環素衍生物,該衍生物也可以以藥丸形式給藥。考慮到這個目標,他於 1996 年與哈佛大學(位於馬薩諸塞州劍橋市)的分子生物學家 Walter Gilbert 共同創立了 Paratek,後者曾獲得 1980 年諾貝爾化學獎的一部分。
在早期,Paratek 與更大的公司建立了合作伙伴關係——德國拜耳公司,然後是默克公司,然後是瑞士巴塞爾的諾華公司。但隨著這些公司轉移重心或監管變化使奧馬環素成為糟糕的財務賭注,每筆交易都解散了。到 2012 年 Loh 被聘用時,Paratek 已經完成了其化合物的 I 期和 II 期臨床試驗,並積累了大量關於其安全性的資料——但它的資金即將耗盡。Loh 將員工人數從約 34 人削減至 6 人,關閉了研究實驗室,而執行團隊則四處奔走籌集資金。他們有九個月沒有領工資。
“我聘請了一位破產律師,為期 18 個月,”他回憶道。“我每週都和他談話。我應該在星期一開門嗎?我是否有足夠的現金這樣做?”
2014 年,Paratek 透過一種稱為反向收購的操作公開上市,將其自身併入一家名為 Transcept Pharmaceuticals 的美國公司,該公司已在納斯達克證券交易所上市,但銷售業績令人失望,並且只剩下一小部分員工。這筆交易為 Paratek 帶來了 1.1 億美元的收入,使其能夠啟動奧馬環素的 III 期臨床試驗並開始謹慎的重新聘用員工計劃。2018 年 10 月,FDA 批准了該藥物的口服和靜脈注射製劑,用於治療兩種疾病:複雜性皮膚感染和社群獲得性細菌性肺炎。22 年的征程結束了——但奧馬環素將要上市的領域仍然很危險。
Loh 是一位心臟病專家,在轉向製藥行業之前,曾在兩家學術醫療中心領導移植專案,他知道這種藥物是需要的。但他意識到這將不容易。
“如果醫院裡沒有抗生素,任何事情都不可能成功,”他說。“你不能做手術。你不能做移植。你什麼都做不了。我們有一種我們相信可以挽救生命的產品。在我們能夠長期取得成功之前,我們的使命還沒有完成。”
有限的壽命
抗生素提出了一個持久的經濟難題。這些藥物改變了世界。然而,儘管它們具有獨特的力量,但自由市場並不重視它們。
原因很複雜。首先從顯而易見的開始:抗生素殺死細菌,細菌是不斷適應威脅其生存的生物。一旦使用一種新化合物,病原體就會開始進化出應對攻擊的策略。這意味著抗生素的有效壽命以及盈利潛力可能是有限的——這種情況在大多數其他藥物中不會發生。
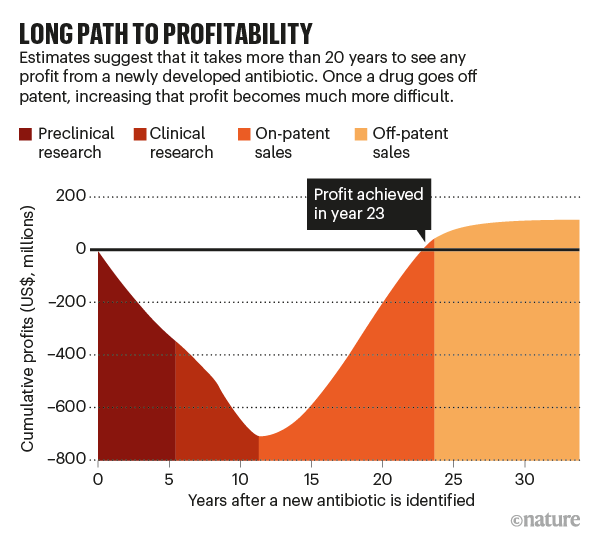
如果一家公司能夠快速銷售大量新抗生素,那麼新抗生素壽命的長短就沒那麼重要了,但結構性和倫理障礙都在阻礙這種情況的發生(見“通往盈利的漫長道路”)。先說結構性障礙。相對較少的患者患有需要用新型抗生素治療的耐藥性感染,而大多數其他藥物類別都用於治療大量人群。美國疾病控制與預防中心估計,美國每年有 280 萬例耐藥性感染。相比之下,美國每天有 740 萬人服用胰島素來治療糖尿病。
圖片來源:Nature;資料來源:“抗生素耐藥性危機”第 1 部分:“原因和威脅”,C. Lee Ventola,《藥房與治療學》,第 40 卷;2015 年 4 月;Axios
據一項估計,一種新型抗生素每年需要至少產生 3 億美元的收入才能實現可持續發展。其他研究人員估計,美國針對耐碳青黴烯類腸桿菌科細菌(最耐藥和最頑固的感染類別之一)的新型抗生素的整個市場每年為 2.89 億美元。
換句話說,“這個市場可能只容得下一家藥物,”Shlaes 說。“如果人們想要獲得投資回報,這個市場容不下不止一家藥物。”
據紐約市投資公司 Needham 的分析,現在生產抗生素的公司中,只有少數幾家每年從抗生素中賺取 1 億美元或更多。其餘大多數公司的年收入在 1500 萬美元到 5000 萬美元之間。
然後是倫理困境。由於細菌暴露於抗生素的任何風險都會導致耐藥性的發展,因此使用該藥物治療一名患者會削弱其未來拯救其他患者的能力。因此,在整個醫療保健領域普遍遵守的規則(統稱為抗生素管理)要求緩慢部署新型抗生素。這在長期內保護了它們的可靠性,但也損害了它們的銷量。例如,在 2018 年,包括最近破產的 Achaogen 公司生產的一種抗生素在內的三種新型抗生素僅在 35% 的符合使用條件的病例中使用。這對於管理來說可能是一次勝利。但對於那些本可以銷售更多藥物的公司來說,這是一個實實在在的損失。
John Rex 是一位醫生和長期藥物開發人員,他是英國曼徹斯特和維也納的抗真菌藥物公司 F2G 的首席醫療官,他用以下方式總結了這個悖論:“發明一種糟糕的抗生素,沒人會用它。發明一種非常好的抗生素,真的沒人會用它。”
走進深淵
組成 Paratek 的 100 人團隊以不安的心情迎來了 2019 年底。他們正盯著 Woodrow 所謂的“商業化深淵:在你真正開始獲得實際銷售額之前,你需要花費大量資金的三年時期”。抗生素的銷量穩步上升,但速度緩慢——當年有望賺取 1300 萬美元。與此同時,Woodrow、Loh 和 Brenner 承諾進行批准後研究和監測,他們估計這將花費 7000 萬美元。而且他們失去了一盞指路明燈:他們的聯合創始人 Levy 於 2019 年 9 月去世。
然後聖誕節提前到來了。美國聯邦機構生物醫學高階研究與開發管理局 (BARDA) 向 Paratek 授予了一份為期 5 年、價值 2.85 億美元的合同,用於為可能接觸到生物武器炭疽的前線部隊採購奧馬環素。(此次採購驗證了 Levy 早先對口服藥物價值的洞察:處於危險中的部隊可以吞下藥丸然後繼續前進,而不是被束縛在靜脈滴注上。)
收到訊息後,Loh 感覺自己終於可以鬆一口氣了。“這是一個巨大的數字——一份禮物,”他不久後說道。“它給了我們時間來獲得發展動力。”
BARDA 的資金就像一座橋樑,跨越了其他公司曾墜入的深淵。在某種程度上,它也證明了激勵措施在修復抗生素市場方面的潛力,美國和歐洲的政策制定者已經對此進行了多年的辯論。激勵措施有兩種型別,分別稱為“推動”和“拉動”。“推動”旨在推動小型公司的新藥候選藥物透過臨床試驗並獲得批准。“拉動”旨在緩解批准後的財務困境,因為此時公司必須在不違反抗生素管理原則的情況下推廣其藥物。
推動激勵措施取得了一些成功。總部位於波士頓大學的非營利組織 CARB-X(抗擊耐藥菌生物製藥加速器)已從美國、英國和其他歐洲政府及慈善機構籌集了約 5 億美元的資金,並正在將這筆資金分配給小型公司。自 CARB-X 於 2016 年成立以來,它已向 67 家公司提供了約 2.5 億美元,以支援有前景的臨床前和 I 期研究。

由於冠狀病毒大流行,許多抗生素供應短缺。圖片來源:Simon Dawson Getty Images
BARDA(也在資助對冠狀病毒疫苗和療法的單獨搜尋)也提供推動贈款,以支援公司進行後期臨床試驗,從而將藥物推向批准。然而,BARDA 與 Paratek 的合同有所不同。它實際上是一種拉動激勵,在奧馬環素獲得批准後,當批准後監測和支援該藥物用於治療其他感染的研究將耗盡微薄的收益時,提供了一筆現金注入。
分析師和立法者等人已經提出了其他形式的拉動激勵措施,美國國會也對其進行了審議,但它們更具爭議性。這些措施包括延長製藥公司擁有的其他藥物成為仿製藥之前的時間(稱為延長市場獨佔期),以及向公司提供數十億美元的市場準入獎勵,使其無需推動其藥物的銷售,否則這會加速耐藥性的發展。另一項擬議的拉動激勵措施——提高美國政府向醫院支付的新型抗生素報銷費用——曾短暫地被新增到為應對冠狀病毒大流行而制定的 2 萬億美元美國刺激法案中。該激勵措施在法案成為法律之前又被取消了。
沒有人找到超越政治現實的道路:在許多選民和政治家眼中,製藥公司是機會主義者,將美國藥品價格抬高到令人無法接受的高度。僅在 2019 年就舉行了多次關於藥品價格的國會聽證會,7 月,唐納德·特朗普總統簽署了幾項旨在壓低價格的行政命令。為任何製藥公司(即使是一家生產急需抗生素的小公司)提供便利都面臨著強大的政治阻力。
Needham 的分子生物化學家和高階分析師 Alan Carr 表示,在支援抗生素研究方面,無論是激勵措施還是投資者,都沒有明確的有效途徑。“對於投資者來說,讓事情變得複雜的是,確實需要新型抗生素——但並非在抗生素的每個領域都需要,”他說。“在某些感染領域,確實存在尚未滿足的需求,我們沒有任何抗生素。然後在其他領域,我們有很多。不幸的是,發生的情況是,投資者將整個領域混為一談。因此,他們不想與其中任何一個領域有任何關係。”
疫情意外
BARDA 合同使 Paratek 從一家銀行存款不足一年的公司變成了一家可以依靠資金維持到 2023 年底的公司。這保證了其眼前的未來,儘管它並沒有解決需要從該藥物中賺取比市場似乎願意支付的更多收益的長期問題。然後冠狀病毒襲擊了。
當 SARS-CoV-2 病例在美國開始增加時,Loh 和他的團隊感到不安。Paratek 的銷售團隊一直在進行正常的拜訪,向傳染病專家和醫院藥劑師解釋奧馬環素,希望它能被管理醫院常規儲備哪些藥物的處方藥委員會選中。他們的工作正在取得成效。一個月又一個月,奧馬環素的銷量增長了 10% 以上。當封鎖開始時,所有這些會議都結束了。該公司擔心其銷量也會停滯不前。但在疫情爆發以來收集的月度資料中,穩步增長仍在繼續。
Paratek 營銷副總裁 Christine Coyne 說:“在封鎖期間,新的處方醫生——我預計這種情況會歸零。”“但我們仍然看到兩位數的增長。”
圖片來源:Nature;資料來源:為後代獲得新藥:藥物管道。《抗菌素耐藥性審查》,2015 年 5 月
現在說是什麼推動了這些銷售還為時過早。現在已經發表了足夠的病例報告,研究人員可以確信細菌性肺炎是 COVID-19 患者的併發症,發生率在 15-20%。在美國部分地區,最常見的細菌性肺炎病原體(肺炎鏈球菌)對阿奇黴素(最常見的仿製抗生素)的耐藥性高達 50%。這可能會推動採用尚未記錄到耐藥性的新藥。其他出版物證實,即使沒有診斷出肺炎,也正在向使用呼吸機的 COVID-19 患者開具大量抗生素(綜述見參考文獻 7)。這是一種針對患者感染醫院獲得性感染的保險政策,而且由於個人防護裝置不足,確認細菌性肺炎所需的程式對於工作人員來說風險太大,無法進行。
作為疫情的副作用,許多其他抗生素也出現短缺。這是國際貿易中斷(大多數抗生素的活性成分來自中國)和國內影響共同作用的結果。例如,在特朗普於 3 月宣佈他支援未經證實且現在基本上已被否定療效的羥氯喹和阿奇黴素組合後,幾家阿奇黴素生產商宣佈,恐慌性購買已引發短缺。
如果這些事件正在提振銷量,那對 Paratek 有利。它們也突顯了 BARDA 合同及時到來的幸運。該公司的供應鏈避開了中國,完全設在歐洲。而且,作為保護國防的一項條件,BARDA 合同中的一項條款要求該公司在美國境內建立一條平行的供應鏈,以避免未來任何疫情爆發造成中斷。
對於 Paratek 團隊來說,奧馬環素對當前危機的適用性驗證了該公司堅持使用其認為需要的產品的承諾。同樣,它也證明了預測緊急情況並在緊急情況發生之前為關鍵醫療干預措施做好準備的重要性。美國在為保護醫護人員免受感染的口罩、呼吸器和其他裝置方面未能做到這一點。它幾乎也未能做到為抗生素的供應做好準備。
“冠狀病毒應該告訴公眾,‘如果你在發生類似事件時沒有現成的技術,你就不能等待一年或兩年——甚至三年或五年——才能把它弄到那裡,’”Loh 說。“你不能在床邊對一家公司說:‘你能今天為我生產這個嗎?’”
本文經許可轉載,並於 2020 年 8 月 19 日在 Nature 首次發表。