公元541年,在與哥特人和汪達爾人進行了多年的戰爭之後,查士丁尼一世皇帝將東羅馬帝國建設成一個龐大的統治區,幾乎環繞地中海。然而,那一年,這位統治者沒有機會慶祝。相反,他受到了一個致命的新敵人的襲擊,一個看不見且難以理解的敵人。
一場神秘的瘟疫席捲了查士丁尼的領土,並進入了他的首都君士坦丁堡。受害者發高燒,腋窩和腹股溝疼痛腫脹,許多人變得神志不清。皇帝本人也病倒了。關於他去世的謠言充滿了恐慌的城市。歷史學家普羅科匹厄斯是該城市的居民,他聲稱在某些日子裡,多達1萬人死亡。查士丁尼設法從瘟疫中倖存下來,但他的帝國在之後多年裡仍然傷痕累累,失去了對許多領土的控制,並努力維持對羅馬的統治。
科學家們一直爭論著這場災難的身份,直到今天。雖然有些人將瘟疫歸咎於鼠疫桿菌的一種特別緻命的菌株——症狀類似於中世紀的黑死病,而鼠疫桿菌是那場災難背後的罪魁禍首——但另一些人則認為查士丁尼受到了一種與臭名昭著的1918年流感大流行相關的流感病毒的襲擊,那次流感大流行估計造成了5000萬至1億人死亡。歷史學家們也想知道這種疾病是從哪裡開始的。許多人將矛頭指向埃及,因為歷史記載表明,在查士丁尼的災難之前,那裡也出現了一種類似的疾病。
支援科學新聞報道
如果您喜歡這篇文章,請考慮透過以下方式支援我們屢獲殊榮的新聞報道 訂閱。透過購買訂閱,您正在幫助確保有關塑造我們當今世界的發現和想法的具有影響力的故事的未來。
現在,生物學家和考古學家聯手從那個時代的牙齒和骨骼中提取古代DNA,已經能夠解決這場長期存在的爭論。牙齒中含有鼠疫桿菌的DNA,而不是流感殘餘物。研究人員追溯這種菌株的時間和全球範圍,瞭解到瘟疫並非始於埃及,而是始於中國西部,並在歐亞草原的高地草原上傳播,然後襲擊歐洲。
德國耶拿市馬克斯·普朗克人類歷史科學研究所的亞歷山大·赫比格說,這種疾病“在羅馬帝國出現之前已經進化了相當長一段時間”,他使用計算機重建了病原體從一個地方傳播到另一個地方時DNA的變化。隨著時間的推移,其中一些變化使病原體能夠在新的宿主中生存和傳播,擴大了其破壞性的範圍。
這種從古代人類遺骸中提取致病微生物DNA的能力,正在幫助填補歷史書中的許多空白。這些分子顯示了我們的歷史是如何被與細菌和病毒的遭遇所塑造的,這些細菌和病毒爆發成大流行病。除了震撼查士丁尼時代的事件外,科學家們還利用病原體DNA來提高我們對黑死病的起源和阿茲特克帝國衰落的理解。他們甚至發現了青銅時代的一種疾病為人們從亞洲湧入歐洲鋪平了道路的證據——而這些人帶來了技術、文化和基因,其影響至今仍可見。
隨著這些發現,關於微生物如何變成瘟疫,出現了一些特定的模式。當微小的生物體遇到密集居住在一起的群體時,它們往往會傳播死亡。它們在以前從未接觸過因此自然免疫力低的人群中迅速傳播。日益增長的國際貿易和人類流動性擴大了傳播範圍,病原體通常會在被社會邊緣化和貧困的人群中發現更高的脆弱性,這些人幾乎沒有資源來保護自己。我們現在再次看到這些模式,因為我們當前由SARS-CoV-2病毒驅動的大流行病正在全球蔓延。
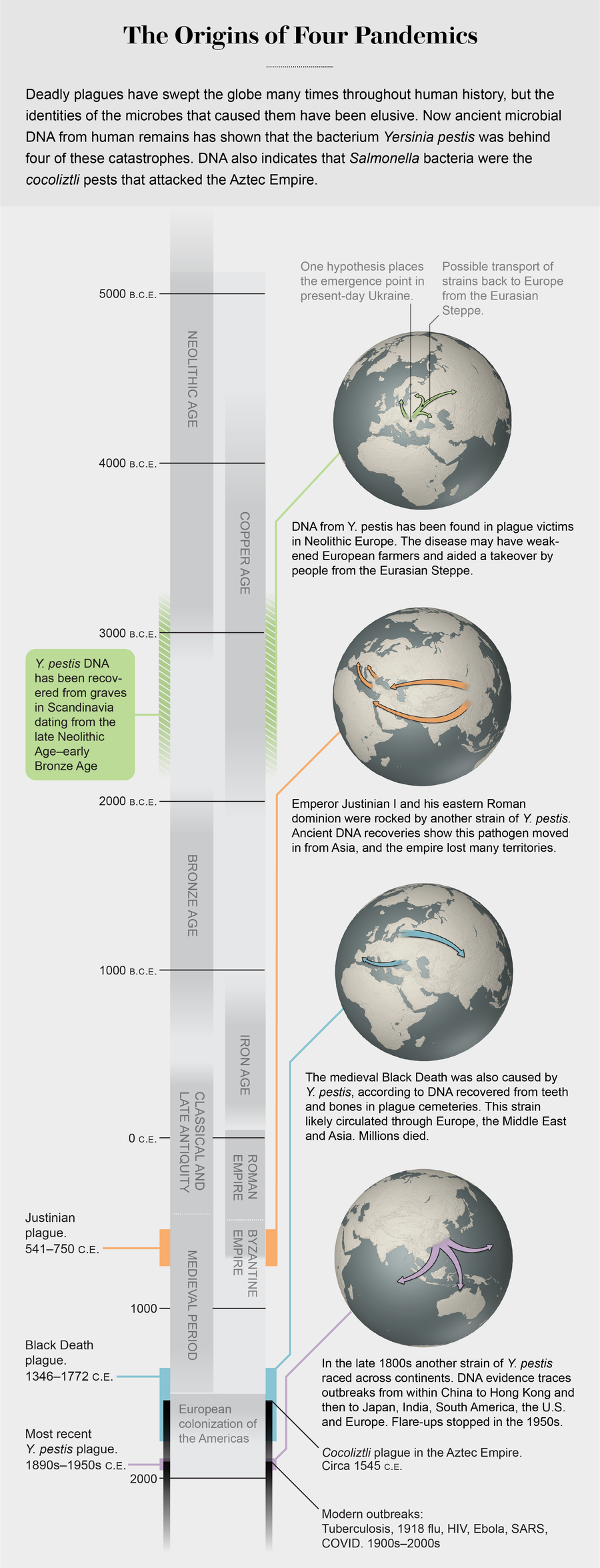
致謝:喬治·雷特塞克(地圖)和珍·克里斯蒂安森(圖表);資料來源:“古代病原體基因組學作為傳染病研究的新興工具”,Maria A. Spyrou等,《自然評論:遺傳學》,第20卷;2019年;“鼠疫桿菌與查士丁尼瘟疫,公元541-543年:基因組分析”,David M. Wagner等,《柳葉刀傳染病》,第14卷;2014年4月;“新石器時代衰落期間鼠疫桿菌基礎譜系的出現和傳播”,Nicolas Rascovan等,《細胞》,第176卷;2019年1月;以及“歷史鼠疫桿菌基因組揭示歐洲黑死病是古代和現代瘟疫大流行的源頭”,Maria A. Spyrou等,《細胞宿主與微生物》,第19卷;2016年6月
分子線索
科學家和歷史學家長期以來一直對將病原體生物學與歷史聯絡起來感興趣,但直到大約十年前,分析古代遺骸(aDNA)中的DNA的困難阻礙了嘗試。例如,從黑死病墓葬中回收病原體基因組的努力只導致了“反覆失敗,反覆失敗,反覆失敗”,安大略省麥克馬斯特大學的aDNA生物學家亨德里克·波伊納哀嘆道。埋葬的骨骼已經退化,只含有極少量的屬於微生物的遺傳分子。
過去十年中的兩項發展改變了局面。一項是考古基因組學專家認識到他們一直在關注骨骼的錯誤部位。牙齒,而不是骨骼,是最好的時間膠囊。在外部,牙齒被堅硬的琺琅質層保護。在內部,牙髓充滿了乾燥的血液——以及血液傳播的病原體的退化殘餘物。科學家可以用牙科鑽鑽出內部,將其溶解,並幸運地發現一些微生物DNA的殘餘物。
但是這些樣本是雜亂無章且支離破碎的。它們仍然需要被縫合回長而詳細的DNA序列中,以便可以將它們識別為屬於特定的細菌或病毒。下一代測序是一種加速這種重組的方法,是第二大進步。由於更強大的計算機,該技術最近得到了廣泛應用,並且“徹底改變了遊戲規則”,波伊納說。基本上,該方法涉及同時並行地對大量短DNA鏈進行測序,並透過在字母序列(熟悉的遺傳密碼A、T、C和G)重疊的地方連線它們,將它們重新組裝成可識別的基因組。這種方法使得從退化的樣本中重建整個基因組成為可能,從而避免了回收罕見的高質量DNA長片段的需要。
更好的樣本和新技術相結合的首批成功案例之一齣現在2011年。波伊納和他的同事從倫敦黑死病墓地獲得的牙齒中回收了一個鼠疫桿菌基因組草圖。他們的發現經過幾十年的推測,證實了這種細菌確實是導致中世紀大流行的罪魁禍首,那場大流行在1347年至1351年間導致30%或更多的歐洲人口死亡。研究人員在接下來的五年裡瞭解到,這種菌株並沒有特別強的毒性;它與現代鼠疫桿菌非常相似,後者遠沒有那麼致命。中世紀的高死亡率似乎是由失控的黑家鼠數量激增所驅動的,黑家鼠在擁擠和營養不良的人群中傳播細菌,這些人群居住在衛生條件惡劣的新興城市中。
也許來自瘟疫aDNA的最大驚喜來自於更早的墓葬。事實證明,無論是查士丁尼瘟疫還是中世紀瘟疫都不是這種微生物首次在跨大陸範圍內改變人類事件。
史前大流行
2015年,從歐亞草原各地埋葬的骨骼中提取的101個古代人類基因組的資料證實,大約5000年前,早期青銅時代的人類,即顏那亞文化,從草原向下遷移,取代了歐洲的新石器時代農業文化。新來者馴養了馬匹和新的冶金形式,並且可能好戰,但大規模的人口轉變仍然讓科學家感到困惑,因為歐洲群體已經繁榮了幾個世紀。“那些組織良好、顯然繁榮的歐洲新石器時代社會怎麼會衰落呢?”參與這項工作的一位考古學家,瑞典哥德堡大學的克里斯蒂安·克里斯蒂安森問道。一些考古證據指向顏那亞人到來前後歐洲農民中普遍存在的人口崩潰,克里斯蒂安森說,他和他的同事開始懷疑是否有一種疾病削弱了歐洲社會,使其足以允許入侵。特別是,他問道:“會不會是黑死病?”
當克里斯蒂安森的團隊對101個古代草原人類基因組進行測序時,他們收集了一切——不僅是人類DNA,還有病毒、細菌和現代環境汙染的混合物。“我們沒有使用的資料佔95%到99%之間,”團隊成員,哥本哈根大學的西蒙·拉斯穆森說。“我們只是把它扔進了垃圾箱。”但到2015年,新的測序技術使他們能夠篩選這些材料,並將其與其他基因組進行比較。“因此,我們收集了所有這些資料——1000億個小的DNA片段——並將它們與瘟疫進行了篩選,”拉斯穆森說。
大約兩週後,科學家的機器得出了答案。大約7%的古代遺骸的牙齒中殘留著瘟疫DNA的痕跡。細菌透過血管進入牙齒,“如果細菌在血液中,那真的非常糟糕”,拉斯穆森說。“這些人很可能死於此。”這種更致命的疾病被稱為敗血性鼠疫;在最常見的型別,腺鼠疫中,細菌感染淋巴結。由於他們檢查的許多aDNA樣本狀況不佳,拉斯穆森還懷疑瘟疫DNA可能在更高比例的材料中存在,但過於混亂而無法檢測到。他認為證據“開始傾向於可能的大流行”。然而,波伊納更為謹慎,並指出除了鼠疫桿菌之外的其他因素——例如饑荒或戰爭——也可能導致歐洲人口崩潰。
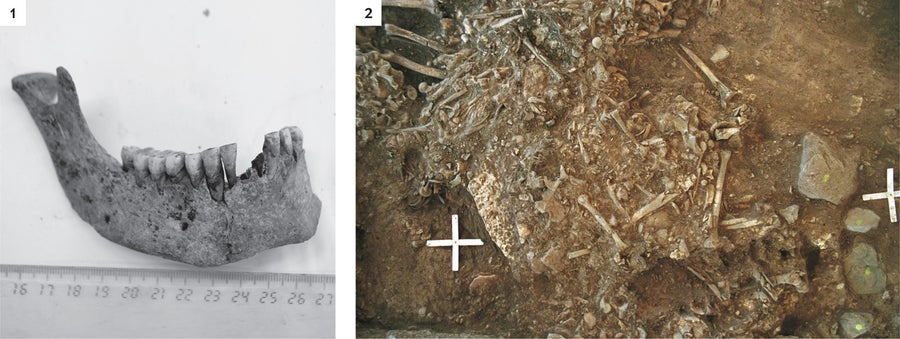
古代細菌DNA在瑞典弗雷爾塞戈登的一個萬人冢中挖掘出的人牙中發現,來自鼠疫微生物鼠疫桿菌(1)。該墓穴大約有5000年曆史,埋葬著大約78人的遺骸(2)。致謝:卡爾-戈蘭·舍格倫(1);攝影:託尼·阿克塞爾松(2)
如果瘟疫桿菌甚至是部分原因,那麼今天就可以看到其影響。克里斯蒂安森的團隊認為,就像後來的鼠疫桿菌爆發一樣,這一次也從草原蔓延到歐洲。如果顏那亞人已經接觸過這種細菌數百年,他們可能對這種細菌具有一定的免疫力。這種抵抗力會使他們相對於遭受瘟疫蹂躪的歐洲農民具有優勢。因此他們遷入了。憑藉更淺的膚色和原始印歐語系,這個群體及其遷徙仍然影響著現代歐洲的外貌、語言和基因。根據克里斯蒂安森的說法,“它改變了歐洲歷史的程序。它改變了歐洲的語言。”他說,從基因上講,歐洲人“是那些草原人的後裔”。
最近,研究小組在瑞典新石器時代的兩具大約五千年前的骨骼中檢測到鼠疫桿菌DNA,從而發現了更多支援這種瘟疫驅動變革理論的證據。看來,這種疾病在顏那亞人入侵之前就已經到達斯堪的納維亞半島。克里斯蒂安森說,他的同事們現在正在“到處搜尋”這種早期變體的其他例項。他稱之為“所有瘟疫之母”。
進化之旅
現在已經分析了數十個古代鼠疫桿菌基因組,來自過去5000年間的各個時間點。這些序列的變化使研究人員能夠重建細菌的進化史,並指出一些早期的基因改變,這些改變可能有助於將一種機會性腸道病原體轉變為人類歷史上最大的殺手之一。
在其最早的形式——5000年前的變體中——細菌不太可能像黑死病版本那樣透過鼠蚤傳播。較老的細菌缺乏現代微生物用來阻止其在跳蚤腸道中消化的酶。它可能是透過宿主——人或動物——咳嗽時透過空氣傳播的液滴傳播的。但在大約4000年前,鼠疫桿菌獲得了一個名為ymt的基因,可能來自另一種腸道細菌。(細菌經常交換基因。)ymt編碼那種保護酶,使瘟疫生物體能夠在跳蚤體內生存並隨昆蟲傳播,馬克斯·普朗克人類歷史科學研究所的古代DNA專家約翰內斯·克勞澤說。
在獲得ymt之後,鼠疫桿菌進化出了形成生物膜的能力——而這種才能或許是微生物最險惡的創新。在一個基因中出現了突變,該基因提高了產生粘性細胞外基質的能力,而其他突變則削弱了通常會減慢或阻止基質產生的不同基因。這些變化使細菌能夠聚結成粘性細胞團。這些細胞團在跳蚤的中腸中積聚,阻塞了其消化道。飢餓的跳蚤被迫瘋狂進食,它們反覆叮咬周圍的任何哺乳動物,並在每次叮咬時傳播細菌。
人類與病原體
aDNA研究使得追蹤除鼠疫桿菌以外的其他微生物的歷史成為可能,使研究人員能夠確定許多現代人類病原體的出現日期,包括麻風病、肺結核、乙型肝炎病毒和細小病毒的菌株,這些病原體是廣泛傳播的麻煩製造者。克勞澤說,這些日期,也許並不令人驚訝,發生在人類開始定居的時候。
隨著文明的發展,遙遠的社群透過馬、車輪,然後是船隻連線起來——無論人們走到哪裡,微生物也隨之而來。赫比格說,長途貿易促進了“全球範圍內的疾病交換”。例如,古代乙型肝炎和瘟疫基因組的分佈與青銅時代和鐵器時代有據可查的人類遷徙路線相符。同樣,威斯康星大學麥迪遜分校的凱特琳·佩珀雷爾說,肺結核是由“羅馬商船的船員或沿著絲綢之路聚集在航點的商人”攜帶的,她的團隊使用肺結核aDNA估計,現代菌株出現的時間不到6000年前——而不是之前認為的7萬多年前。
傳播這些微生物的不僅僅是貿易。病原體通常會利用多種動物宿主,DNA資料表明,當我們與某些動物的關係變得更加密切時,病原體很快就會隨之而來。例如,英國紅松鼠的最後倖存種群之一仍然攜帶中世紀的麻風病菌株,可能是維京皮毛商人運到英格蘭的。同樣,從一具千年歷史的秘魯骨骼的aDNA中顯示,一種感染人類的肺結核菌株顯然是由海豹帶到南美洲的。該肺結核基因組與現代海豹和海獅中發現的菌株最密切相關。“對於這個人群來說,從考古學和人類學的角度來看,這很有道理,因為他們進行了大量的海豹狩獵,”參與這項研究的赫比格解釋說。“他們製作的陶器上可以找到人們狩獵海豹以及加工海豹肉的影像。”
當歐洲人首次抵達時,這種增加對病原體易感性的人類因素——更大的人口、更大的全球連通性、與動物世界不斷變化的關係——對新大陸產生了重大影響。16世紀初,以墨西哥為中心的阿茲特克帝國遭到一小隊西班牙軍隊的入侵,他們在心懷不滿的臣民和競爭對手國家的幫助下推翻了這個文明。然後,西班牙人建立了一個殘酷的委託監護制,即嚴厲的待遇、過度勞累和營養不良。歐洲外來者似乎也帶來了其他襲擊者。
在1521年的最初征服之後,阿茲特克人口遭受了歷史上最嚴重的大流行病之一的摧毀。西班牙方濟各會修士貝納迪諾·德·薩哈貢在最初的西班牙接觸八年後抵達墨西哥,他的書面記載表明,一種感染殺死了高達80%的土著人口。但是,這種當地人稱之為cocoliztli pest的疾病的身份仍然是一個謎。猜測範圍從出血性流感到瘧疾到傷寒再到天花。對於歷史學家來說,甚至不清楚這種疾病是當地起源還是由西班牙人傳入的。
然而,在2018年,aDNA指向了一個可能的罪魁禍首。克勞澤和他的同事從cocoliztli時代萬人冢中發現的骨骼中提取DNA,確定超過一半的樣本含有C型副傷寒沙門氏菌,這是一種引起嚴重腸道疾病的細菌。在歐洲人接觸之前,美洲從未發現過沙門氏菌,因此它幾乎可以肯定是從舊世界運來的。征服者可能在他的跨大西洋船隻上攜帶了受汙染的食物和水,以及其他潛在的傳播媒介,如雞、豬、牛和老鼠等害蟲。所有這些都能夠傳播疾病。
就在這個時候,美洲的一場環境災難幫助沙門氏菌等微生物找到了新的家園。2000年釋出的樹木年輪資料表明,16世紀墨西哥遭受了一系列災難性的乾旱,糧食短缺和人口流離失所使人們身體虛弱,無法抵抗他們免疫系統沒有準備好的陌生微生物入侵者。一個文明崩潰了。
今天,社會對病原體以及如何對抗病原體的瞭解比500年或5000年前的人們要多得多。但是,我們目前與COVID-19的鬥爭表明,我們對新型疾病的脆弱性並沒有改變:它們經常從其他物種跳到人類身上,透過全球貿易和旅行傳播,並因擁擠、貧困和營養不良而加劇。aDNA研究提醒我們這些持久的事實,並表明歷史上一些最大的事件不僅僅是由查士丁尼一世皇帝或征服者埃爾南·科爾特斯等有權勢的人物定義的。它們也深刻地受到他們的帝國幫助傳播的微生物的影響。