75 歲的佩德羅·R·L 在完成六個漫長的化療療程後,收到了他和家人一直期盼的訊息:他的慢性淋巴細胞白血病已完全緩解。但是,當他的身體還在恢復時,他感染了 COVID-19。2021 年 1 月 30 日,他被送入馬德里基隆薩盧德大學醫院。初步治療失敗,到 2 月 25 日,他已發展為重症肺炎。那時,他的醫生巴勃羅·吉薩多建議他們嘗試 普立得辛,這是一種強效抗病毒化合物,正處於治療住院 COVID 患者的 3 期臨床試驗中。
普立得辛來自鮮有製藥商預測到的地方:西班牙伊維薩島西南海岸附近無人居住的埃斯韋德拉島周圍的海底。早在 1988 年,總部位於馬德里的製藥公司 PharmaMar 組織了一次前往這個傳說中的地點的探險,這是一個突兀的露頭,據認為啟發了荷馬在《奧德賽》中關於歌唱美人魚引誘水手走向死亡的故事。科學家們在佈滿紫色珊瑚和紅色海扇的珊瑚礁上潛水時,從 36 米深的岩石斜坡上拉出了一種相對平淡無奇的無脊椎動物——一種半透明的淡黃色海鞘,Aplidium albicans,它看起來像一團廢棄的面巾紙。
研究人員對海鞘很感興趣,因為它們透過不斷地將水吸入桶狀身體中來濾食浮游生物。它們會連同食物一起吸入病毒和其他病原體,因此它們需要強大的化學防禦能力來抵抗傳染性生物——這使它們成為有希望的藥物來源。
支援科學新聞報道
如果您喜歡這篇文章,請考慮透過以下方式支援我們屢獲殊榮的新聞報道 訂閱。透過購買訂閱,您正在幫助確保有關當今塑造我們世界的發現和想法的具有影響力的故事的未來。
到 1990 年,PharmaMar 從 A. albicans 標本中分離出一種對癌細胞和病毒培養物均具有活性的化合物。PharmaMar 追求癌症方向,因為癌症藥物往往比抗病毒藥物更有利可圖。經過數十年的研究和測試,澳大利亞於 2018 年批准普立得辛作為多發性骨髓瘤的治療藥物。
當 COVID 大流行來襲時,該公司科學家迅速證明普立得辛在實驗室培養物和小鼠中均對 SARS-CoV-2 有效,並且在臨床前、頭對頭試驗中優於競爭性抗病毒藥物。2020 年,PharmaMar 啟動了一項針對住院 COVID 患者的 1-2 期臨床試驗,該試驗於 2021 年結束。結果令人矚目:74% 的中度疾病患者在首次給藥後一週內完全康復。3 期試驗預計將於 12 月完成。今年 5 月,PharmaMar 的病毒學醫學主管 Jose Jimeno 表示,普立得辛似乎優於其他 COVID 抗病毒藥物。* 普立得辛對佩德羅·R·L 的影響令人印象深刻;經過兩個療程的治療,他的肺炎和其餘症狀已完全清除。

冷凍架存放著 30 多年來收集的 18,000 株微生物菌株。科學家們在培養物中培養菌株,測試它們的生物特性,並可能對其基因組進行測序,以尋找可利用的基因。圖片來源:Devin Oktar Yalkin
如今,在全球範圍內,有 21 種已獲批准的藥物來源於海洋,其中大多數是從無脊椎動物中分離出來的。另一種海鞘,Ecteinascidia turbinata,它附著在水下紅樹根上,產生了分子混合物,從而產生了 Yondelis,一種肉瘤和卵巢癌藥物,以及 Zepzelca,一種靶向小細胞肺癌的藥物。一種覆蓋日本南部潮汐池岩石的黑色海綿,Halichondria okadai,產生了一種藥物,現在以 Halaven 的名義銷售,用於治療晚期乳腺癌。而來自芋螺(Conus magus)的毒液肽,則促成了 Prialt,一種慢性疼痛藥物。
珊瑚、海蛞蝓、海洋蠕蟲和軟體動物也產生了有希望的化合物。“在過去的 6 億年中,這些無脊椎動物一直生活在像培養皿一樣的微生物湯中,”康奈爾大學海洋生態學家德魯·哈維爾說,他解釋了它們對強大防禦能力的需求。平均一升海水中含有約 10 億個細菌和 100 億個病毒。儘管科學家最初認為大多數海洋無脊椎動物進化出了自己的武器,但他們在過去幾十年中瞭解到,這些防禦性物質中的大多數實際上是由共生生活在這些生物組織內的微生物產生的。例如,去年,佐治亞理工學院的薩馬爾·阿卜杜勒拉赫曼領導的一個團隊測試了來自紅海的五種海蛞蝓,並發現了產生抗菌、抗真菌和抗癌劑的細菌。
藥物發現科學家——幾十年來,他們一直專注於陸地生物學,因為它更熟悉且更容易獲取——現在普遍認識到,微生物主導著海洋的生物多樣性,是最有可能的海洋衍生藥物來源。目前正在進行臨床試驗的 23 種新藥中,有 16 種是由微生物產生的,另外 4 種來自無脊椎動物,這些無脊椎動物的復原能力可能歸功於共生微生物。近年來,科學家們已從海洋微生物中分離出數千種有希望的化合物,其多樣性反映了海洋條件的巨大變異性。“在陸地上,微生物會乾涸;它們難以維持體液平衡,”哈維爾說。“但海洋是一個更加寬鬆、更受歡迎的環境。”
然而,對於大多數已獲批准的海洋藥物而言,這個過程耗時數十年,部分原因是資金不足,部分原因是分離、測試和生產大量新型化合物非常耗時。幸運的是,基因組學、化學和計算領域的最新進展使科學家們能夠在從海洋中尋找救命藥物時更有針對性和效率。
基因靶點
1989 年,保羅·詹森將來自巴哈馬海底的沉積物帶回他在斯克裡普斯海洋研究所的實驗室,以從中挖掘具有醫學用途的細菌。這並不容易。他的第一個挑戰是在實驗室條件下培養海洋細菌,而實驗室條件充其量只是海洋環境的近似。然後,當某些物種生長時,他必須說服它們至少產生一些武器庫中的分子,即使它們沒有受到自然環境中面臨的相同刺激。
儘管存在這些障礙,詹森最終還是發現了一種新的細菌物種,Salinispora tropica,它產生了一種新型的癌細胞殺傷分子。該化合物現在以 marizomib 的名義銷售,剛剛完成了一項針對膠質母細胞瘤(一種奪去了約翰·麥凱恩和博·拜登生命的致命腦癌)藥物的 3 期試驗。目前正在等待美國食品和藥物管理局的批准。Marizomib 是海洋細菌具有產生新藥潛力的有力例證,但這個過程花費了三十多年,這促使詹森和其他人尋找更好的方法。
到 2000 年代初期,基因組學已經改變了他們的工作。包括 S. tropica 在內的海洋微生物的第一個完整基因組序列顯示,在實驗室培養物中僅產生少量化合物的物種通常可以產生更多化合物;它們中的一些物種的 DNA 中有數十個化合物編碼基因簇。幾年之內,宏基因組學——對樣品中整個生物群落的 DNA 進行測序的過程——揭示了更多隱藏的潛力。科學家們開始在他們甚至沒有在實驗室中培養過的物種中發現化合物編碼基因簇。
今天,詹森也在直接尋找分子,而不是產生它們微生物。在過去一年中的四個場合,他團隊的博士後研究人員涉足聖地亞哥洛馬岬半島附近的海草床,將微小的吸附珠片(稱為樹脂)浸入水中,這些樹脂可以將有機分子從海水中吸出。回到實驗室後,詹森分析樣品中的生物活性化合物——可以作用於活生物體的化學物質。

保羅·詹森(左圖)數十年來一直致力於研究海洋化合物以尋找潛在藥物。他實驗室的一位研究人員(右圖)正在浸入一塊鑲有吸附樹脂珠片的薄片,這些珠片可以從海水中吸出有機分子。圖片來源:Devin Oktar Yalkin
他已經有了一個突破:一種具有不尋常碳骨架的化合物,其中包括一組詹森認為可以“像彈頭一樣”發揮作用的酶反應分子。這種新型結構的功能可能與現有藥物非常不同。“我認為它會殺死細胞,”詹森預測。“現在我們希望瞭解它的靶點可能是什麼。”
接下來,他需要將化合物與其生產者匹配起來。巨大的海洋微生物基因組和生物活性化合物資料庫,以及關聯它們所需的計算能力,使科學家能夠有效地將化學物質與基因聯絡起來。格拉斯哥斯特拉斯克萊德大學的海洋微生物化學家凱瑟琳·鄧肯是這種方法的先驅,她稱之為基於模式的基因組挖掘。該技術最近才成為可能。“我們只是沒有工具來比較如此規模的資料集,”她說。
鄧肯現在正在使用這項技術來分析從南極洲海岸外 4,000 至 4,500 米深的海底拉出的深色沉積物巖芯。早期結果令人興奮:樣品包括至少兩種新的海洋細菌物種,Pseudonocardia abyssalis 和 Pseudonocardia oceani,它們產生抗菌化合物。在陸地上,同屬的成員與真菌種植螞蟻共生,產生抗菌和抗真菌分子,以阻止病原體侵入螞蟻的真菌花園。不難想象,海洋表親可能會產生抗感染藥物。
鄧肯和詹森等科學家面臨的最大挑戰之一是弄清楚哪些分子發現值得最多關注。德國蒂賓根大學的微生物學家納丁·齊默特開發了一種工具,透過尋找抗性基因來幫助研究人員以更有針對性的方式挖掘基因組。任何產生有毒分子的生物體都必須具有某種保護自身免受自身武器攻擊的機制——通常是透過製造毒素細胞靶點的修飾副本,使其能夠抵抗其攻擊。
齊默特的工具名為“抗生素抗性靶點搜尋器”,它允許研究人員訪問包含 10,000 多個細菌基因組的資料庫——或上傳他們自己的基因組——並執行搜尋與特定細胞功能相關的抗性基因。隨著資料庫的增長,它將變得更有價值,尤其是在研究人員加速工作以對來自極端、未充分探索環境的物種的基因組進行測序時。齊默特的靶點搜尋器已顯示出如此大的前景,以至於初創公司 Hexagon Bio 構建了一個類似的工具來挖掘真菌基因組以尋找有希望的化合物。
新型抗生素
有針對性的基因組挖掘正當其時。COVID 大流行凸顯了對更深層次的藥物庫以治療新出現的傳染病的需求。對治療已確立疾病的新藥也存在迫切需求。許多細菌感染,包括肺炎、肺結核、淋病、敗血症和各種食源性疾病,由於微生物對抗生素的耐藥性日益增強,變得越來越難以治療——在某些情況下,甚至不可能治療。公共衛生官員普遍認為抗生素耐藥性是人類面臨的最嚴重的威脅之一。
由於幾乎所有抗生素都來自陸地微生物,因此似乎很明顯,海洋微生物(人們對它們的研究嚴重不足)有可能解決這場危機。悉尼大學化學家理查德·佩恩對它們治療肺結核(由 Mycobacterium tuberculosis 引起)的能力特別興奮。“在過去 10 年中,肺結核一直是傳染病中最大的殺手,”佩恩說,“而且隨著所有用於 COVID 的努力,我們在肺結核控制方面倒退了。”需要一種靶向與過去藥物不同的結核病蛋白質的抗生素。
這正是佩恩在韓國濟州島新陽海灘(一個以理想的帆板運動和風箏衝浪條件而聞名的小半島上的白色沙灘馬蹄形海灣)的一種細菌中發現的。該化合物 ohmyungsamycin A 阻止 M. tuberculosis 正確處理其廢物蛋白質,最終殺死細胞。當佩恩建立了一組化學類似物——略有改變、化學合成的分子,可以批次生產——其中一種非常有效,以至於它在三天內完全滅菌了實驗室培養的結核病菌落。該藥物已被證明對受感染的斑馬魚有效,並且正在進入小鼠試驗階段。
在最近幾十年中,尋找和開發新抗生素在很大程度上已落到學術界身上,因為這些藥物的售價如此之低,以至於製藥公司缺乏追求它們的經濟動機。同樣的道理也適用於治療許多被忽視的熱帶疾病,包括瘧疾。2012 年,斯克裡普斯化學家威廉·格威克從庫拉索港口船隻繫泊繩索上生長的一簇藍藻中分離出一種名為 carmaphycin B 的分子。他化學合成了 一組類似物,並針對癌細胞對其進行了測試,這是研究的常用第一步。

最近,一艘潛水器在南加州附近深海(水下 2,500 米)捕獲了一種海洋無脊椎動物,它仍處於冷凍狀態,等待鑑定。圖片來源:Devin Oktar Yalkin
結果並不出色,因此格威克將注意力轉向了其他專案。然而,最近,一位同事建議他們對瘧疾寄生蟲測試他的類似物,而這次的結果令人震驚。“其中一種對瘧疾的反應非常靈敏,”格威克說。而且,它對人體細胞沒有毒性。
格威克現在有資金探索 carmaphycin B 作為一種新型抗瘧疾藥物。無論它最終是否成為一種獲批藥物,這一發現都提醒人們,科學家們已經鑑定的數千種生物活性海洋化合物中蘊藏著可能性。
Carmaphycin B 也提醒人們,僅靠技術進步並不能帶來新藥;通常需要的是偶然性和利用偶然性的意願。在格威克的前學生喬肖娜·努內利從繫泊繩索上收集藍藻的當天,她本應在其他地方潛水。但是當她的實驗室夥伴和潛水夥伴感染了登革熱時,她不得不取消那些計劃,轉而在研究站附近浮潛。
隨著對海洋探索的投資增加,利用這種偶然性的機會也在增加。在最近一次前往中太平洋鳳凰群島的施密特海洋研究所研究船“法爾科”號上的探險中,安娜·戈蒂埃成為首批從該群島採集深海細菌樣本的科學家之一。戈蒂埃是哈佛大學的博士生,她計劃在探險期間進行免疫反應實驗,因此她沒有立即冷凍她從海中提取的細菌,這是通常的做法。相反,她開始在船上培養這些生物。
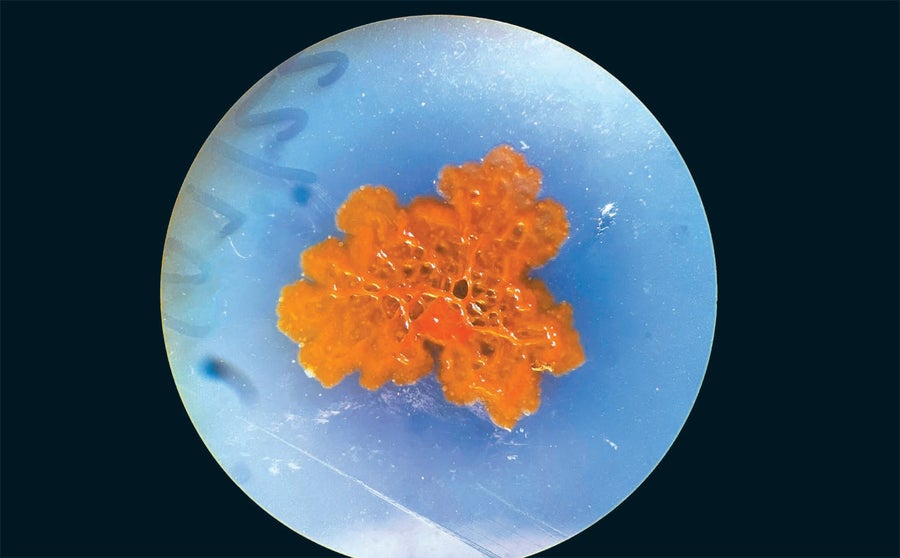
來自海洋的 Salinispora 細菌在實驗室培養皿中培養,產生一種名為 marizomib 的癌細胞殺傷分子,該分子剛剛完成作為膠質母細胞瘤(一種致命的腦癌)藥物的 3 期試驗。圖片來源:Devin Oktar Yalkin
該技術提供了一個意想不到的好處:存活率遠高於傳統的、基於實驗室的解凍標本培養物。她培養的 80% 的細菌與哺乳動物通常遇到的細菌差異很大,以至於它們沒有引發哺乳動物細胞的免疫反應。這一發現雖然離取得醫學進展還很遠,但對免疫療法和疫苗具有誘人的潛力。
新救命藥物的希望,加上日益嚴重的公共衛生危機,為格拉斯哥的鄧肯等科學家提供了巨大的動力。“我認識一些人,他們一直在使用最後一道抗生素,但產生了耐藥性,”她說。“我的祖母死於敗血症。每個人都有這樣的故事。”
鄧肯希望這些故事可能會在未來十年內發生改變。“海洋環境非常未被發現,”她驚歎道。下一個普立得辛就在海洋中。它可能已經在實驗室裡了。
*編者注(2022 年 11 月 18 日):此句子在釋出後經過編輯,以更正 Jose Jimeno 在 PharmaMar 的職位描述。

