凱瑟琳·納格勒小時候吃雞蛋會起蕁麻疹。她對青黴素有反應。大學畢業後在實驗室工作時,她對小鼠產生了嚴重的過敏反應,導致喘息、腫脹和呼吸困難——兩次被送進急診室。
今天,納格勒是芝加哥大學的免疫學家,她正在幫助開創一個新興的研究領域:研究如何利用腸道細菌來幫助食物過敏患者。
激發她興趣的並非個人的過敏經歷。相反,是她在 1980 年代作為博士生時的一個奇怪的觀察。她當時正在研究免疫系統失調並攻擊關節內膠原蛋白的實驗鼠,這會導致嚴重的關節炎。科學家可以透過在皮膚下注射膠原蛋白來快速引發這種疾病。但是,奇怪的是,當納格勒後來餵食這些動物膠原蛋白,使用一根蛇形管子插入它們的胃中時,卻產生了相反的效果:小鼠的情況好轉了。
支援科學新聞報道
如果您喜歡這篇文章,請考慮透過以下方式支援我們屢獲殊榮的新聞報道 訂閱。透過購買訂閱,您正在幫助確保有關塑造我們當今世界的發現和想法的有影響力的故事的未來。
幾十年後,這種被稱為口服免疫療法的概念已作為食物過敏的治療方法投入使用,食物過敏影響了美國估計 3200 萬人,其中包括每個教室大約兩名學童。在過去的十年左右,一些過敏症專科醫生已經開始使用少量、定期的致敏食物(或其製品)來治療食物過敏患者,以平息過敏反應。隨著一月份美國食品和藥物管理局批准了一種標準化版本——一套治療花生過敏的每日膠囊——這種方法有望越來越受歡迎,美國食品和藥物管理局批准了第一種治療兒童花生過敏的藥物。
但口服免疫療法也有缺點。治療方案可能令人緊張,因為它涉及每天食用可能致命的食物。它並非對每個人都有效,並且對解決根本疾病幾乎沒有作用。成功主要意味著能夠安全地吃下幾個花生,例如,而不是對一丁點花生粉產生反應。
對於一些家庭來說,這種適度的進步改變了生活。然而,它仍然是不穩定的:患者必須每天或每週幾次食用少量該食物,才能終生保持療效——否則他們可能會失去保護。
因此,納格勒和其他幾位研究人員正在努力尋找更輕鬆、更持久地治療食物過敏的方法。他們的目標是他們認為的根本原因——有益細菌群落或微生物組的失衡,微生物組存在於我們的腸道中——希望以此來重置免疫系統。
生產基於微生物組的治療方法將具有挑戰性,有許多細節需要解決,例如提供哪些微生物以及如何最好地輸送它們。但這種方法正在獲得動力。去年,納格勒的團隊和波士頓的另一個小組報告了一項重要的進展:他們透過提供來自健康、非過敏人類嬰兒的腸道微生物,預防了易過敏小鼠的嚴重過敏反應。“資料是可靠的,而且非常令人鼓舞,”克利夫蘭診所的兒科過敏症專科醫生傑克琳·比耶拉克說。
3 月份,科學家報告稱,在過敏患者的胃和腸道中發現了大量針對花生過敏原的抗體,進一步支援了胃腸道是食物過敏調節和治療熱點的觀點。目前,多家公司正在測試幾種策略。
長期以來,人們一直困惑為什麼一個人可以耐受某種食物,而另一個人卻會過敏,但正如納格勒在她與人合著的《免疫學年度評論》文章中概述的那樣,她確信微生物組是關鍵。
假設的誕生
完成研究生工作四年後,納格勒開始在哈佛醫學院運營一個實驗室。那時她研究的是炎症性腸病,而不是食物過敏。但隨著 1990 年代的研究表明,炎症性腸病主要是由針對腸道細菌的免疫反應引起的,她將注意力轉向了微生物組。
然後在 2000 年,她偶然看到了一篇有趣的出版物。它描述了一種花生過敏小鼠模型,該模型模仿了人類經歷的關鍵症狀。小鼠不停地抓撓。它們的眼睛和嘴巴變得浮腫。有些小鼠會呼吸困難——一種危及生命的過敏反應,稱為過敏性休克。
.jpg?w=900)
圖片來源:Getty Images
所有這些都發生在研究人員餵食小鼠花生粉之後。“這引起了我的注意,”納格勒說。這與她早期對關節炎小鼠的研究結果相反,在關節炎小鼠的研究中,餵食膠原蛋白平息了免疫反應。為什麼會有差異?
另一份報告顯示,花生過敏小鼠存在一種基因缺陷,該缺陷會損害一種名為 TLR4 的受體,該受體位於免疫細胞膜中並識別微生物。看起來花生過敏小鼠缺乏腸道微生物和免疫細胞之間發生的正常對話。
“那是我的靈光一閃時刻,”納格勒說。也許生活在我們體內的數萬億微生物透過刺激 TLR4 受體來抑制對食物的免疫反應。也許這種熙熙攘攘的微生物組的擾動改變了抑制作用並導致過敏症的上升。
這個想法與歷史趨勢相吻合。隨著社會現代化,人們搬到城市地區,更多地進行剖腹產,服用更多抗生素,並食用更多加工過的低纖維食物——所有這些都會擾亂微生物組。這些生活方式轉變的時間與觀察到的食物和其他型別過敏症的增加相吻合,這些過敏症在一代人中的急劇上升指向了一些環境原因。
.jpg?w=900)
2004 年,納格勒和她的同事發表了一份報告,表明花生僅在 TLR4 受體突變的小鼠中引起過敏性休克,而不是在 TLR4 正常的基因相關品系中引起過敏性休克。當科學家用抗生素消滅腸道細菌群時,這種差異消失了。然後,即使是正常小鼠也變得容易患上食物過敏症,這意味著細菌是保護的核心。
從那時起,納格勒的實驗室一直在努力確定哪些細菌是有益的,並瞭解它們如何調節過敏反應。
早期影響
在他們的工作中,納格勒的團隊專注於梭狀芽孢桿菌和擬桿菌——人類腸道中兩大類細菌。該團隊與在無菌環境中繁殖的小鼠合作,因此根本沒有微生物組,他們發現,當將梭狀芽孢桿菌而不是擬桿菌引入到這些非常乾淨的小鼠的腸道中時,它們可以預防食物過敏反應。
有一種可能的解釋:定植了梭狀芽孢桿菌的小鼠具有更多的調節性 T 細胞,這是一種抑制免疫反應的細胞。梭狀芽孢桿菌小鼠還產生了更多的稱為 IL-22 的分子,該分子可增強腸道內壁。一種新的理論開始出現:如果缺乏保護性微生物,腸道屏障會減弱,從而使食物蛋白質滲入血液並可能引發過敏反應。
這種推理與一個奇怪的觀察結果非常吻合,即主要的食物過敏原(在牛奶、雞蛋、花生、堅果、大豆、小麥、魚和貝類中發現的某些蛋白質)彼此之間幾乎沒有生化相似性。它們的共同點是能夠在消化道中保持完整,消化道通常將食物分解成小塊,然後人體將其吸收為營養。納格勒說:“花生似乎正是憑藉其在腸道中抵抗降解的能力才成為佼佼者。”
研究進一步鞏固了腸道細菌與食物過敏之間的聯絡,並表明微生物組的影響發生在生命早期。研究人員分析了健康嬰兒和患有雞蛋或牛奶過敏的嬰兒的糞便,結果表明,過敏和非過敏嬰兒的腸道細菌群落不同。
另一項研究跟蹤了 226 名患有牛奶過敏症的兒童,從嬰兒期到 8 歲。科學家發現,某些細菌,包括梭狀芽孢桿菌,在最終擺脫過敏症的 3 至 6 個月大嬰兒的糞便樣本中含量更高,而那些仍然過敏的嬰兒則不然。科學家們在年齡較大的嬰兒中沒有看到這些群體之間的相同差異,這表明過敏保護性微生物可能只在生命早期起作用。
“所有這些都指向了預防方面的機會視窗的概念,”該研究負責人,紐約市西奈山伊坎醫學院的兒科過敏症專科醫生蘇平達·布尼亞瓦尼奇說。
因果證據
從出生起,我們的免疫系統就接受了生死攸關的選擇教育。它們學會了殺死細菌、腫瘤和垂死的細胞。它們還必須學會對周圍環境中的許多其他事物視而不見——神經纖維、骨組織、零食時間食用的牛奶和餅乾中的蛋白質。納格勒實驗室和另一個團隊在 2019 年發表的小鼠研究令人信服地論證了腸道微生物培養了這種關鍵的免疫決策能力。
在其中一項研究中,納格勒和同事收集了健康和牛奶過敏嬰兒糞便中的腸道細菌,並將這些微生物集合放入無菌小鼠的消化道中。他們發現,來自健康嬰兒的腸道細菌保護了小鼠免受牛奶過敏反應,而來自過敏嬰兒的微生物則沒有。
該團隊使用數學和計算機科學技術分析結果,確定了存在於健康嬰兒而非過敏嬰兒中的細菌菌株。他們還檢查了腸道內壁細胞中的基因活動——某些基因模式是健康腸道屏障的特徵——並尋找了其存在與健康屏障相關的微生物。
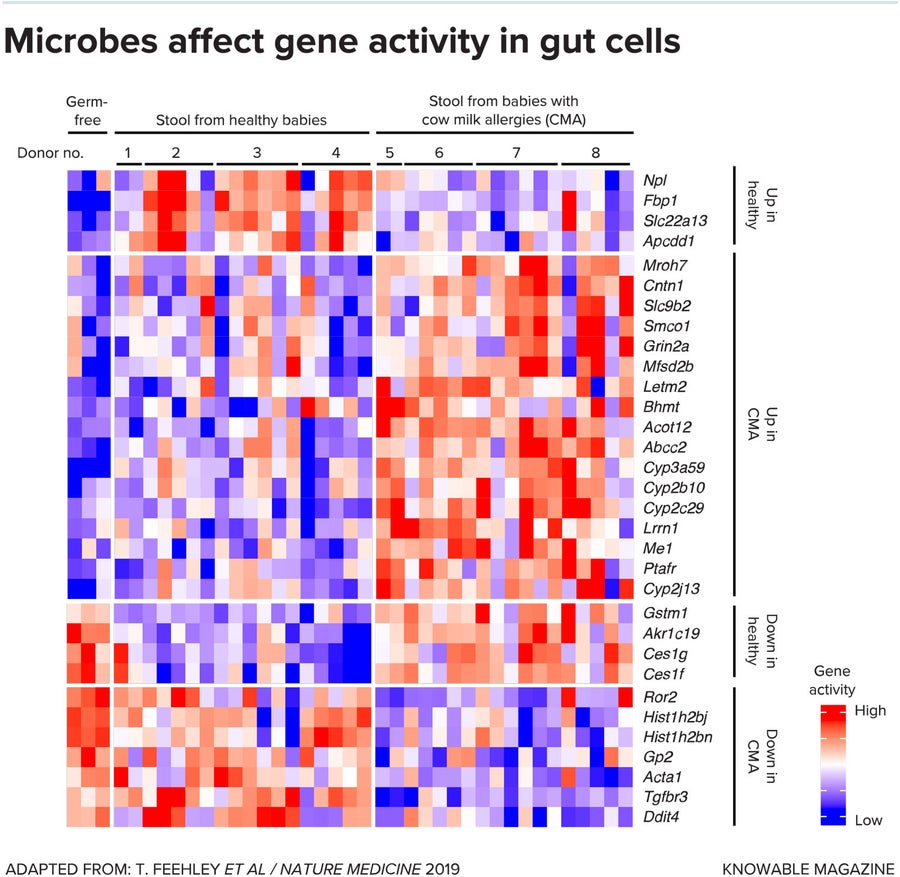
一種梭狀芽孢桿菌,Anaerostipes caccae,從這兩項分析中脫穎而出。當科學家們將A. caccae單獨轉移到無菌小鼠體內時,它似乎模仿了完整、健康的微生物組所賦予的保護作用。
另一個團隊由波士頓兒童醫院的裡瑪·拉希德和塔拉爾·查蒂拉領導,他們使用了類似的方法,使用了高度過敏的小鼠,發現單一物種Subdoligranulum variabile和一組梭狀芽孢桿菌物種預防了過敏反應。調節性 T 細胞是反應的關鍵,並在微生物的刺激下開始發揮作用。
科羅拉多大學丹佛分校的研究飲食學家卡琳娜·文特爾說,這些研究和其他研究清楚地表明,微生物組對於預防食物過敏和誘導耐受性非常重要,她正在研究孕婦懷孕期間的飲食、嬰兒的微生物組與溼疹和過敏風險之間的聯絡。但是,她說,“就多樣性和特定菌株而言,微生物組應該是什麼樣子,我們根本不知道。”
試驗和問題
許多未知因素給希望開發更好的食物過敏治療方法的研究人員留下了一個難題:是提供完整、健康的微生物組更好,還是僅僅補充一些有益的微生物更好?“我每天都在撓頭思考這個問題,”拉希德說。
她正在領導一項臨床研究,以測試第一種可能性。在這項小型的試驗中,花生過敏的成年人將吞服含有來自健康捐贈者的全套腸道細菌的藥丸,這些捐贈者由非營利性糞便庫 OpenBiome 預先篩選以確保安全。這種方法被稱為糞便移植,尚未獲得 FDA 批准,但越來越多地用於治療嚴重的腸道疾病,目的是透過輸注健康、平衡的微生物組來修復患病的微生物組。
其他試驗也在進行中。Pareto Bio(位於加利福尼亞州拉霍亞)正在利用波士頓團隊確定的保護性菌株,開發一種活微生物產品來治療食物過敏。另一家公司,Vedanta Biosciences(位於馬薩諸塞州劍橋市)正在開發一種益生菌膠囊,其中包含精選用於誘導調節性 T 細胞的梭狀芽孢桿菌菌株的混合物。Vedanta 正在測試這些膠囊作為花生過敏成年人口服免疫療法的附加療法。
第三家公司 Prota Therapeutics(位於澳大利亞墨爾本)正在將一種類似的策略商業化,即將花生口服免疫療法與益生菌相結合——在他們的情況下,是一種常用於治療胃腸道問題的乳桿菌菌株。
從捐贈者那裡施用完整的微生物組並非沒有風險:已有四名患者因與糞便移植相關的嚴重感染住院,其中一人死亡。因此,一些研究人員認為,最好使用精確定義的物種。雖然這可能會削弱益處,“但您不太可能引起意想不到的問題,”馬薩諸塞州總醫院食物過敏中心主任韋恩·施雷弗勒說,他正在領導 Vedanta 研究。
但是,所有微生物組調節方法都面臨著一個共同的挑戰:當某人已經存在微生物組時,即使是不健康的微生物組,如何建立新的微生物。傳統上,患者會接受抗生素治療,以幫助新細菌站穩腳跟。但也許還有另一種方法。納格勒與芝加哥大學生物分子工程師傑夫·哈貝爾共同創立的一家初創公司 ClostraBio 正在開發一種將活細菌與關鍵微生物代謝物丁酸鹽相結合的療法。
已知該化學物質可增強腸道屏障功能,並且可能還具有抗菌作用,這可能有助於為新增的微生物創造生態位。ClostraBio 計劃在 2021 年前啟動首次人體試驗,納格勒說。
在未來幾年,研究人員將更多地瞭解如何利用微生物組來對抗食物過敏。這並非易事。遺傳、飲食、環境暴露:所有這些都會影響過敏風險。“這是一個很大的難題,”布尼亞瓦尼奇說。微生物組只是其中的一塊——但她、納格勒和其他人都在押注它將成為重要的一塊。
本文最初發表於Knowable Magazine,它是 Annual Reviews 旗下的獨立新聞事業。註冊新聞通訊。
