早在最早的動物在遠古地球被水覆蓋的表面遊動之前,生命史上最重要的相遇之一就發生了。一種原始細菌被我們最古老的祖先——一個單獨的、自由漂浮的細胞吞噬。兩者融合形成了一種互惠互利的關係,這種關係已經持續了十億多年,後者提供了一個安全、舒適的家,前者變成了一個動力源,為維持生命所必需的過程提供能量。
這是迄今為止關於被稱為線粒體的細胞成分或細胞器如何形成的最好假設。今天,數萬億個這樣的細菌後代生活在我們體內,產生 ATP,這種分子能量來源維持著我們的細胞。儘管線粒體與人體機制密不可分地結合在一起,但它們也保留了其細菌過去的殘餘物,例如它們自己的 DNA 組。
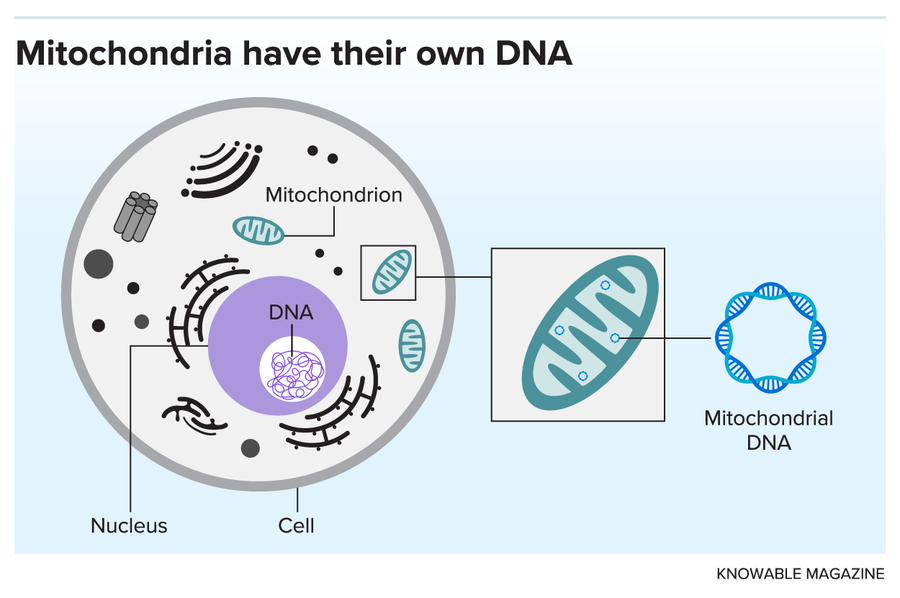
構成人類基因組的 DNA 包含在我們細胞的細胞核中。但線粒體擁有自己的環狀 DNA 組,這很可能是它們古代細菌過去的殘餘物。
支援科學新聞事業
如果您喜歡這篇文章,請考慮透過以下方式支援我們屢獲殊榮的新聞事業 訂閱。透過購買訂閱,您正在幫助確保未來能夠繼續講述關於塑造我們當今世界的發現和思想的具有影響力的故事。
這些特徵使線粒體既成為我們細胞的關鍵要素,又成為潛在問題的來源。與構成人類基因組的細胞核內的 DNA 一樣,線粒體 DNA 也可能攜帶突變。年齡、壓力和其他因素可能會擾亂線粒體的許多功能。最重要的是,線粒體損傷會釋放分子,由於它們與細菌產生的分子相似,可能會被我們的免疫系統誤認為是外來入侵者,從而引發針對我們自身細胞的有害炎症反應。
似乎有一個器官特別容易受到線粒體損傷:我們能量需求旺盛的大腦。“細胞的能量需求越高,它們擁有的線粒體就越多,線粒體健康就越關鍵——因此出現問題的可能性就越大,”美國國家神經疾病與卒中研究所 (NINDS) 研究神經退行性疾病的博士後研究員安德魯·默爾曼 (Andrew Moehlman) 說。據估計,每個神經元最多可以有 200 萬個線粒體。
一小部分但數量不斷增長的科學家現在正在將注意力轉向線粒體對大腦健康的貢獻。對人類和實驗動物的研究——儘管其中大部分仍處於初步階段——表明,這些細胞器可能是幾乎所有型別腦部疾病的關鍵因素,包括神經發育障礙(如自閉症)、精神疾病(如抑鬱症和精神分裂症)以及神經退行性疾病(如帕金森病)。它們甚至可能處於研究腦部疾病的研究人員長期存在的謎團的核心:遺傳易感性和環境影響如何相互作用,使人們面臨患上這些疾病的風險。
動力源的問題
在 20 世紀 60 年代,研究人員發現線粒體擁有一組獨特的遺傳物質。調查顯示,線粒體 DNA 像細菌的 DNA 一樣,形成一個環狀鏈,僅編碼 37 個基因——僅佔人類基因組中數萬個基因的一小部分。
不久之後,在 20 世紀 70 年代,耶魯大學的一名博士生道格拉斯·華萊士 (Douglas Wallace) 對線粒體 DNA 產生了興趣。華萊士推斷,由於線粒體是人體能量的主要生產者,因此其 DNA 的突變會導致疾病。“當時沒有人認為這是合理的,”他說。直到 1988 年,華萊士和他的同事首次建立了線粒體 DNA 突變與人類疾病之間的聯絡——萊伯氏遺傳性視神經病變,一種導致突發性失明的疾病——醫學研究人員才開始認真對待這個想法,華萊士回憶道。
此後,研究人員已將數十種疾病與線粒體 DNA 和與線粒體功能相關的核 DNA 的改變聯絡起來——有趣的是,其中大多數疾病要麼是神經系統的,要麼對大腦有一定影響。華萊士現在是費城兒童醫院線粒體和表觀基因組醫學中心主任,他有一個簡單的解釋:儘管大腦僅佔人體重量的 2%,但它卻消耗了大約五分之一的身體能量。華萊士說,就像高能電器在城市停電期間電壓水平下降時會受到不成比例的影響一樣,即使線粒體功能略有下降,也可能對大腦產生巨大影響。
華萊士對線粒體如何可能導致自閉症譜系障礙特別感興趣。幾個研究小組的研究表明,線粒體疾病,即由細胞器缺陷引起的一系列症狀,在自閉症患者(5%)中比一般人群(約 0.01%)更為普遍。另有 30% 到 50% 的自閉症兒童表現出線粒體功能障礙的跡象,例如細胞呼吸產生的某些副產物水平異常,而細胞呼吸是 ATP 的產生過程。
在一些自閉症患者中,科學家已經發現了線粒體 DNA 或人類基因組中已知影響線粒體功能的大約一千個基因中的一些基因的遺傳差異。還需要做更多的工作來確定這些遺傳變異是否真正導致或促成了自閉症,但最近一項對小鼠的研究暗示可能存在聯絡。華萊士及其同事今年早些時候在PNAS 上報告說,線粒體 DNA 中的特定突變可能導致小鼠出現類似自閉症的特徵,包括社互動動受損、膽怯和強迫行為。
遺傳改變並不是線粒體可能導致自閉症的唯一途徑。某些環境因素,如有毒汙染物,也與患上這種疾病的較高風險有關。亞利桑那州鳳凰城兒童醫院的兒科神經學家和自閉症研究員理查德·弗萊 (Richard Frye) 及其同事發現,這些因素也可能擾亂自閉症患者線粒體的健康。在一項研究中,他們發現自閉症兒童出生前接觸的空氣汙染量會改變其線粒體產生 ATP 的速率。在另一項研究中,研究人員發現早期接觸營養金屬(如鋅)以及有毒金屬(如鉛)與這些細胞器在日後患有自閉症的人體內的功能之間存在相關性。弗萊說,總而言之,這些發現表明,線粒體可能是自閉症與導致該疾病的環境影響之間缺失的環節。
“現在就對很多事情做出任何確定的結論還為時過早,但看起來很多自閉症兒童的線粒體都受到了破壞,”弗萊說。“環境暴露,尤其是早期暴露,可能會對線粒體進行程式設計,使其具有不同型別的呼吸生理學特徵。”
研究人員還在精神分裂症和抑鬱症患者中發現了線粒體功能障礙的跡象,例如它們代謝糖產生能量的方式紊亂。此外,研究還表明,線粒體可能對許多精神疾病的風險因素敏感:早年生活的心理壓力。例如,童年時期經歷過創傷事件的人,每個細胞似乎擁有更多的線粒體基因組。布朗大學的生物精神病學研究員特蕾莎·丹尼爾斯 (Teresa Daniels) 說,線粒體 DNA 的這種增加(可能表明新線粒體的形成)可能是為了補償細胞器中的問題,她正在努力解決這個問題。丹尼爾斯是 2020 年發表在臨床心理學年度評論 上的一篇論文的合著者,該論文討論了線粒體在精神疾病中的作用。
托萊多大學研究腦部疾病的醫生科學家羅伯特·麥卡勒姆斯密斯 (Robert McCullumsmith) 說,儘管線粒體功能障礙似乎出現在多種腦部疾病中,但尚不清楚這些細胞器的缺陷是這些疾病的主要原因還是次要影響,但他並未參與線粒體方面的研究。“這有點像先有雞還是先有蛋的問題,”他說。然而,麥卡勒姆斯密斯補充說,研究線粒體在這些疾病中的作用非常重要,他看到了有希望的證據表明,即使不能治癒這些疾病,靶向線粒體的療法最終也可能使患者受益。
當朋友變成敵人
當線粒體受損或功能失調時,一個後果僅僅是 ATP 減少,因此大腦正常運作的能量也減少。但線粒體可能導致腦部疾病的另一種方式源於它們的祖先歷史。
作為細菌的後代,線粒體具有 DNA 和其他成分,當細胞受傷或受到壓力時,這些成分會被釋放出來,並被我們的免疫系統誤認為是外來威脅。2010 年,哈佛大學的研究人員報告稱,嚴重身體損傷(如車禍造成的骨折或出血)患者的血液中會迅速釋放線粒體 DNA。反過來,這會吸引免疫細胞並引發嚴重的炎症反應,類似於敗血症——一種危及生命的疾病,免疫系統會攻擊人體自身的組織。
幾年後,當時在耶魯大學做博士後的 A·菲利普·韋斯特 (A. Phillip West) 及其同事表明,即使在沒有如此嚴重的損傷的情況下,例如當細胞器缺乏關鍵蛋白質時,DNA 也可能從線粒體中洩漏出來並激活免疫系統。
越來越多的研究表明,線粒體 DNA 釋放引起的炎症可能導致神經退行性疾病(如帕金森病、阿爾茨海默病和肌萎縮側索硬化症 (ALS))中發現的損傷。在不同的研究方向中,科學家已將這些疾病與炎症以及無法正確清除細胞中缺陷線粒體聯絡起來。線粒體引發的炎症可能是兩者之間缺失的環節。
例如,與某些形式的遺傳性帕金森病相關的兩個基因——PINK1 和 PRKN 中的突變——會導致受損線粒體被分解和從細胞中清除的過程出現問題。2019 年,NINDS 的理查德·尤爾 (Richard Youle) 領導的一個小組證明,在 PINK1 和 PRKN 突變的小鼠中,誘導線粒體損傷(透過精疲力竭的運動或改變線粒體 DNA)會啟用炎症分子。這些動物的大腦中也失去了產生多巴胺的神經元,並出現運動問題——這是帕金森病的標誌。然而,當研究人員對經過基因改造而缺乏重要炎症分子的小鼠重複實驗時,這些影響並未發生。總之,這些發現表明,在基因上易患帕金森病的動物中,壓力或線粒體 DNA 中的故障都可能引發促進該疾病的炎症。
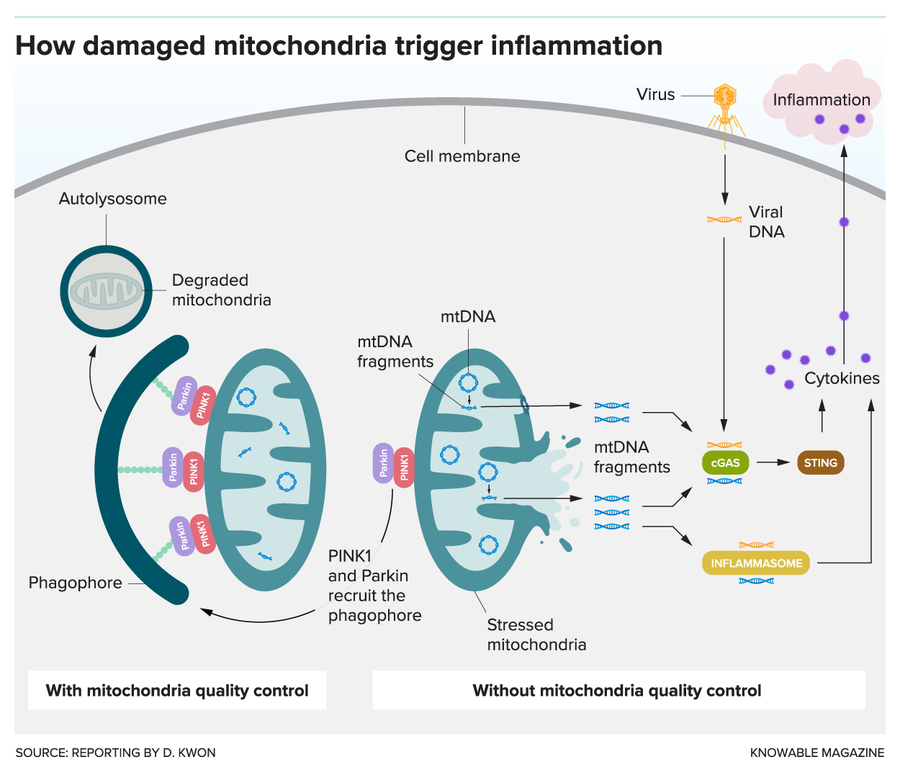
細胞具有多種質量控制機制來去除功能失調的線粒體。一種重要的機制涉及 Parkin 和 PINK1 蛋白。當線粒體受損時,PINK1 和 Parkin 會募集吞噬泡,吞噬泡會吞噬細胞器並開始降解過程。當這種質量控制系統失效時,受損的線粒體 DNA (mtDNA) 可能會從線粒體中逃逸。(這種情況是如何發生的仍然是一個懸而未決的問題,但它可能透過特殊孔隙或線粒體膜的破裂而逸出)。一旦釋放,mtDNA 片段可以啟用 cGas-STING 或炎症小體等分子,這兩者都可以感知來自病毒和其他入侵者的外來 DNA。反過來,這可以增加細胞因子的產生並引起炎症。
雖然還需要做更多的工作來確定人類是否也會發生相同的過程,但“有很多證據表明,未能維持健康的線粒體是導致帕金森病症狀發展的早期病理事件之一,”默爾曼說,他與尤爾合著了 2020 年發表在細胞與發育生物學年度評論 上的一篇論文,該論文討論了線粒體問題如何可能導致神經退行性疾病。
隨著線粒體 DNA 洩漏是不祥之兆的證據越來越多,一些研究人員正在將注意力轉向原因。現在是德克薩斯農工大學免疫生物學家的韋斯特說,可能有很多過程在起作用。他說,一種情況是,細胞器隨著時間的推移不斷釋放低水平的 DNA——當遺傳或環境因素加劇這種情況時,這種積累可能會達到疾病發生的閾值。
心理壓力可能是其中一個因素。在 2019 年的一項研究中,哥倫比亞大學的線粒體心理生物學家馬丁·皮卡德 (Martin Picard) 及其同事報告說,在簡短的公開演講任務中,參與者被要求為自己辯解,反對一項所謂的過錯,之後血液中游離的線粒體 DNA 水平升高,表明線粒體已經釋放了它們的遺傳物質。
韋斯特說,這種線粒體損傷和 DNA 釋放可能會導致人類疾病,即使在沒有感染的情況下,炎症也似乎在其中發揮作用,例如癌症、自身免疫性疾病和神經退行性疾病。
他和其他人也懷疑線粒體引起的炎症可能是衰老本身的關鍵驅動因素。在最近的一項研究中,韋斯特的團隊證明,經過基因改造使其線粒體 DNA 不穩定的小鼠衰老得更快,出現了脫髮和骨質流失等問題,並且過早死亡。消除由線粒體 DNA 啟用的免疫系統元素逆轉了這一過程,將動物的壽命延長了約 40 天。(這些結果在 bioRxiv 上發表,尚未經過同行評審。)韋斯特說,如果未來的研究證實這一點,它將提供證據表明,至少在這些小鼠中,衰老部分是由線粒體損傷驅動的。
多用途線粒體
線粒體還具有其他功能,有助於維持健康的大腦功能——或者在功能失調時引起問題。例如,線粒體有助於控制細胞代謝的潛在有毒副產物(稱為活性氧)的平衡,以及皮質醇等應激激素的合成。線粒體也具有高度動態性——透過訊號分子和物理連線相互通訊。它們不斷經歷裂變(一個大的線粒體分裂成兩個小的線粒體)或融合(當它們結合時)。研究人員才剛剛開始意識到,這些持續的相互作用也可能以各種方式影響大腦功能和行為。
瑞士聯邦理工學院的行為神經科學家卡門·桑迪 (Carmen Sandi) 及其研究小組檢查了具有高焦慮樣行為的小鼠的線粒體,例如不太願意在開放區域度過時間。他們發現,在這些動物中,與表現出較低焦慮水平的動物相比,伏隔核(一個參與獎勵處理的大腦區域)神經元中的線粒體在產生 ATP 方面不太擅長。高焦慮動物也表現出較低水平的融合酶——這種酶使線粒體能夠結合並混合其內容物,以便在需要時相互支援。研究人員發現,提高這種蛋白質的水平不僅恢復了線粒體功能,還減少了焦慮行為。
諸如此類的發現讓科學家有理由希望,他們有一天能夠開發出針對這些細胞器的腦部疾病治療方法。例如,弗萊最近開始了一項臨床試驗,以調查營養補充劑是否可以逆轉他的團隊在自閉症兒童身上發現的線粒體異常。華萊士補充說,研究人員已經知道許多潛在的治療方法,可以幫助增強線粒體的功能——從藥物到行為干預,例如運動。
測試此類干預措施需要時間。目前,科學家們正忙於解開線粒體在大腦中具有的多種功能。這項工作的大部分仍處於初步階段,但來自包括神經科學、免疫學和心理學在內的各個學科的證據讓科學家們對未來感到興奮。桑迪說,關於線粒體的新發現還有很多空間。“我認為它們的作用遠不止神經科學家過去認為的那樣。”
10.1146/knowable-061621-1
本文最初發表於 Knowable Magazine,這是 Annual Reviews 的一項獨立新聞事業。註冊新聞通訊。